| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《物质结构和元素周期律》高频试题特训(2019年最新版)(十)
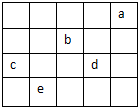 参考答案:由表中元素的位置关系,可知:a为氦,b为氧,c为硅,d为氯,e为砷. 本题解析: 本题难度:简单 5、选择题 下列各组大小顺序不正确的是( ) 参考答案:A.S2-和Cl-具有相同的核外电子排布,都有3个电子层,原子核外电子排布相等的离子,核电核数越大,离子半径越小,则有S2->Cl-,Na+和Mg2+具有相同的核外电子排布,都有2个电子层,离子半径Na+>Mg2+,故有S2->Cl->Na+>Mg2+,故A正确; 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《氧化还原反.. | |