1、选择题 一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
A.2.5mol C
B.2 mol A、1 mol B和10 mol He(不参加反应)
C.1.5 mol B和1.5 mol C
D.2 mol A、3 mol B和3 mol C
参考答案:A、B
本题解析:A正确,该反应为等体积反应,在恒温恒容的条件下,投料量成比例达平衡时即为等效平衡,平衡后各组分的百分含量相同;所以,加入2.5mol C与加入3mol C互为等效平衡,而3molC又相当于加入2molA和1molB;起始时加入2 mol A和2 mol B与加入1 mol A和1 mol B互为等效平衡,所以,当再加入1molA时,平衡后A的体积分数大于a%;B正确,10 mol He为无气体,不影响平衡移动,所以2 mol A、1 mol B和10 mol He相当于加入2 mol A、1 mol B,其理由与A一样;C错,1.5 mol B和1.5 mol C相当于加入1 mol A和2 mol B,而开始时充入2 mol A和2 mol B与开始时充入1 mol A和1 mol B互为等效平衡,则加入1 mol A和2 mol B,又相当于在开始时充入1 mol A和1 mol B基础再加入1 mol B,则平衡时A的体积分数小于a%;D错,2 mol A、3 mol B和3 mol C相当于加入4 mol A和4 mol B与开始时充入2 mol A和2 mol B互为等效平衡,即平衡后A的体积分数为a%
本题难度:困难
2、选择题 在某温度下,可逆反应mA+nB?pC+qD平衡常数为K,下列说法正确的是( )
A.K越大,达到平衡时,反应进行的程度越大
B.K越小,达到平衡时,反应物的转化率越大
C.K随反应物浓度的改变而改变
D.K随着温度的升高而增小
参考答案:A
本题解析:
本题难度:一般
3、选择题 关节炎病因是在关节滑液中形成尿酸钠晶体,尤其在寒冷季节能诱发关节疼痛,其化学机理为:①HUr(尿酸)+H2O?Ur-(尿酸根离子)+H3O+;②Ur-(aq)+Na+?(aq)?NaUr(s).下列对反应②的叙述中正确的是( )
A.反应的△H<0
B.降低温度,平衡向逆反应方向移动
C.反应的△H>0
D.升高温度,平衡向正反应方向移动
参考答案:由题目信息可知,关节炎病因是在关节滑液中形成尿酸钠晶体,尤其在寒冷季节能诱发关节疼痛,说明温度越低,越有利于尿酸钠的形成,温度降低平衡向正反应进行,降低温度平衡向放热方向移动,故反应②是放热反应,即△H<0,升高温度平衡向逆反应方向移动,故BCD错误、A正确,故选A.
本题解析:
本题难度:简单
4、填空题 现有反应:mA(g)+ B(g) 2C(g),达到平衡后,当升高温度时,A的转化率变小;当减小压强时,混合体系中C的质量分数不变,则:
2C(g),达到平衡后,当升高温度时,A的转化率变小;当减小压强时,混合体系中C的质量分数不变,则:
(1)该反应的△H?0(填“>”或“<”),且m?1(填“>”“=”“<”)。
(2)若加入B(假设容器的体积不变),则A的转化率?,B的转化率?。 (填“增大”“减小”或“不变”)
(3)若B是有色物质,A、C均无色,则加入C(假设容器的体积不变)时混合物颜色?,而维持容器内压强不变,充入氖气时,混合物颜色?(填“变深”“变浅”或“不变”)。
(4)一定温度下,向1L密闭容器中加入1mol C(g)使其分解,气体A的物质的量随时间的变化如下图所示。则0~2 min内的平均反应速率υ(C)=?。
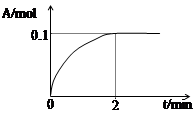
参考答案:(1) <;=?(2)增大?减小?(3)变深?变浅?(4)0.1mol・L-1・min-1
本题解析:减小压强是C的质量分数不变,确定左右化学计量数之和相等,m=1;加入C时平衡左移颜色加深,维持压强不变,充入氦气容器体积膨胀,气体浓度减小颜色变浅。由图像不难确定C的反应速率。
本题难度:一般
5、填空题 工业上制取三氧化硫反应的热化学方程式为:
2SO2(g)十O2(g) 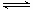 2SO3(g) △H=-198kJ・mol-1
2SO3(g) △H=-198kJ・mol-1
(1)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 (填序号)。
A.每生成1mol SO3的同时生成0.5mol O2
B.容器中混合气体的密度不变
C.SO2、O2、SO3的物质的量之比为2:1:2
D.容器中气体总压强不变
(2)400℃,1.01×105Pa下,上述反应中n(SO3)和n(O2)随时间变化的关系如图所示。下列叙述正确的是 (填序号)。
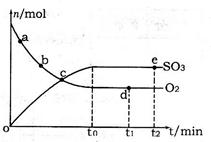
A.点a的正反应速率比点b的大
B.点c处反应达到平衡状态
C.点d和点e处的n(O2)相同
D.500℃,1.01×105Pa下,反应达到平衡时,n(SO3)比图中e点的值大
(3)已知该反应的K(400℃)=7200mol-1・L。在400℃时,容积为1.0L的密闭容器中充入0.05mol SO2(g)和0.03mol O2(g),反应一段时间后,有0.04mol SO3生成。此时,该反应 (填“是”、“否”或“无法判断”)达到化学平衡状态,理由是 。
参考答案:(1)AD(2分)(2)AC(2分)
(3)否(2分),400℃时,浓度熵Q=1600mol-1・L,而K(400℃)=7200mol-1・L,Q<K,反应没有达到平衡状态;(2分)
本题解析:(1)A、每生成1mol SO3的同时生成0.5mol O2,说明正逆反应速率相等,反应达到平衡状态,故A正确;B、容器是恒容的,无论反应是否达到平衡状态,混合物的质量始终不变,容器的体积不变,导致密度始终不变,所以不是达到平衡状态的标志,故B错误;C、SO2、O2与SO3的物质的量之比为2:1:2,这与反应的初始物质的量以及反应的转化程度有关,不能确定是否达到平衡,故C错误;D、该反应是一个反应前后气体体积改变的化学反应,当反应达到平衡状态时,各物质的量不变,导致容器中压强不随时间的变化而改变,故D正确;故选:AD;
(2)A.反应物浓度越大,反应速率越快,故a点时刻的正反应速率比b点时刻的大,故A正确;B.a、b、c三点未到达平衡状态,反应向正反应进行,故B错误;C.d、e两点处于平衡状态,温度相同,C(O2)相等,n(O2)相同,故C正确;D.该反应正反应是放热反应,升高温度平衡向逆反应移动,平衡时三氧化硫的物质的量减小,故D错误;故答案为:AC;
(3) 2SO2(g)十O2(g)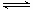 2SO3
2SO3
起始(mol/L) 0.05 0.03 0
反应(mol/L) 0.04 0.02 0.04
一段时间后(mol/L)0.01 0.01 0.04
400℃时,浓度熵Q=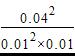 =1600mol-1・L>K(400℃)=7200mol-1・L,反应没有达到平衡。
=1600mol-1・L>K(400℃)=7200mol-1・L,反应没有达到平衡。
考点:考查化学平衡常数及化学平衡状态的判断、化学平衡图象。
本题难度:困难