1、选择题 对于达到平衡状态的可逆反应:N2+3H2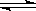 2NH3(正反应为放热反应)下列叙述正确的是
2NH3(正反应为放热反应)下列叙述正确的是
A.反应物和生成物的浓度相等
B.N2和H2的浓度之比一定为1:3
C.降低温度,平衡混合物里NH3的浓度增大
D.增大压强,不利于氨的合成
参考答案:C
本题解析:略
本题难度:一般
2、填空题 (5分)在一定体积的密闭容器中,进行如下化学反应:其化学平衡常数K与温度t的关系如下:CO2(g)+H2(g) 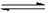 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t(℃)
| 700
| 800
| 830
| 1000
| 1200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
请回答下列问题:
(1)该反应的化学平衡常数K =?。
(2)该反应为?反应(填“吸热”或“放热”)。
(3)800℃,固定容器的密闭容器中,放入混合物,其始浓度为c(CO) =" 0.01" mol/L, c(H2O) =" 0.03" mol/L, c(CO2) =" 0.01" mol/L,c(H2) =" 0.05" mol/L,则反应开始时,H2O的消耗速率比生成速率? __ _(填“大”、“小”或“不能确定”)。
(4) 830℃,在1L的固定容器的密闭容器中放入2 mol CO2和1 mol H2,平衡后CO2的转化率为? _____,H2的转化率为? ________。
参考答案:(1) K=c(CO)・c(H2O)/c(CO2)・c(H2)?(2)吸热?(3)小?(4) 1/3,?2/3
本题解析:(1)化学平衡常数:在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值。故该反应的化学平衡常数为K =c(CO)・c(H2O)/c(CO2)・c(H2)
(2)随着温度的升高,平衡常数越来越大,说明反应向正反应方向进行,故改反应为吸热反应。
(3)由投放物的浓度可知,相当于多投了H2,故反应向正反应方向进行,H2O的消耗速率比生成速率小。
(4)CO2(g)+H2(g) 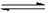 CO(g)+H2O(g)
CO(g)+H2O(g)
始态? 2? 1? 0? 0
反应? a? a? a? a
终态 2-a? 1-a? a? a
830℃时的平衡常数K=1.0,故得K=a.a/(2-a)(1-a)=1?即a=2/3,故平衡后CO2的转化率为
(2/3)÷2=1/3,H2的转化率为(2/3)÷2=2/3
点评:此题考核了平衡常数的定义及算法,学生只要理解了平衡常数,就能较好的做此类题,难度不大。
本题难度:一般
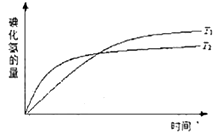
3、选择题 在密闭容器中进行如下反应:H2(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示,符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示,符合图示的正确判断是
A.T1>T2,△H>0
B.T1> T2,△H<0
C.T1<T2,△H>0
D.T1< T2,△H<0
参考答案:D
本题解析:温度越高,化学反应速率越大,达到平衡用的时间越少,曲线的斜率越大,所以T1<T2;升高温度,化学平衡向吸热反应方向移动,导致产物的量降低,说明该反应向逆反应方向移动,所以逆反应方向是吸热反应,正反应是放热反应,即正反应的△H<0,故选D.
本题难度:一般
4、填空题 将CH4与H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g),将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,平衡常数K=27,此时测得CO的物质的量为0.10mol,求CH4的平衡转化率.
参考答案:依据化学平衡的三段式列式计算,设CH4与H2O(g)物质的量为a,
?CH4(g)+H2O(g)?CO(g)+3H2(g)
起始量(mol)?a?a?0?0
变化量(mol)?0.10?0.10?0.10?0.30
平衡量(mol)?a-0.10?a-0.10?0.10?0.30
由平衡常数表达式:K=C(CO)C3(H2)C(CH4)C(H2O)=0.10mol/L×(0.30mol/L)3C(a-0.10)mol/L×C(a-0.10)mol/L=27
解之得:a=0.11?
平衡转化率:0.100.11×100%=91%?
故答案为:91%
本题解析:
本题难度:一般
5、填空题 在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
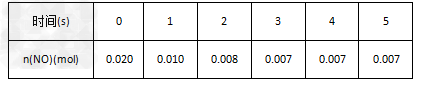
(1)NO的平衡浓度c(NO)=?。
(2)用O2表示从0~2s内该反应的平均反应速率v= ? 。
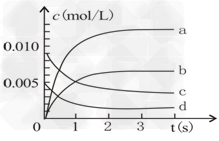
(3)下图中表示NO2变化的曲线是? 。
(4)800℃时,容器内起始压强和平衡后压强之比为___________________。
参考答案:(1)3.5×10-3mol・L-1 ?
(2)1.5×10-3mol・L-1・s-1
(3)b ?
(4)3:2.35
本题解析:
本题难度:一般