1、填空题 (14分)下图是一个化学过程的示意图。已知甲池的总反应式为: 2CH3OH+3O2+4KOH?2K2CO3+6H2O?填写下列空白:

(1)请写出甲、乙两池的名称。甲电池是?,乙池是?。
(2)甲池中通入CH3OH的电极名称是?,电极反应方程式为?;乙池中B(石墨)电极的名称是?。
(3)电解过程中,乙池溶液pH的变化为(“升高”、“降低”或“不变” )?。
(4)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O?2?mL(标准状况下)
参考答案:(14分)
(1)原电池、电解池
(2)负极、CH3OH - 6 e- + 8OH― = CO32― + 6H2O?阳极
(3)降低
(4)280
本题解析:略
本题难度:一般
2、选择题 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是(? )

A.液滴中的Cl-由a区向b区迁移
B.液滴边缘是正极区,发生的电极反应为O2+2H2O+4e-=4OH-
C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e-=Cu2+
参考答案:B
本题解析:液滴边缘O2多,发生正极反应O2+2H2O+4e-=4OH-。液滴下的Fe发生负极反应Fe-2e-=Fe2+,为腐蚀区(a)。A项错误,Cl-由b区向a区迁移;C项错误,液滴下的Fe因发生氧化反应而被腐蚀;D项错误,Cu不如Fe活泼,作正极,负极反应为Fe-2e-=Fe2+。
本题难度:一般
3、选择题 我们在学习和生活过程中所观察的以下现象与电化腐蚀有关的是
A.光亮的自行车钢圈不易生锈
B.炒过菜的铁锅未及时洗净出现红褐色锈斑
C.光亮的铜丝在火焰上灼烧后变黑
D.实验室镁带拆封放置一段时间后表面变灰暗
参考答案:B
本题解析:自行车钢圈属于合金,不易生锈;铜加热时被氧化生成黑色氧化铜;镁是活泼的金属,极易被氧化,这些都是与电化学腐蚀无关系的。选项B中是钢铁的电化学腐蚀,所以答案选B。
本题难度:简单
4、简答题 钢铁工业是国家工业的基础.请回答钢铁冶炼、腐蚀、防护过程中的有关问题.
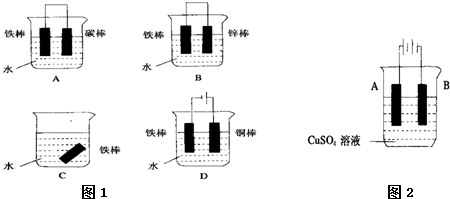
(1)图1中下列哪个装置可防止铁棒被腐蚀______.
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图2,请回答:
①A电极对应的金属是______(写元素名称).
②B电极电极反应式______.
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因______.
参考答案:(1)在B原电池装置中,正极金属铁被保护,在电解池装置D中,阴极铁金属被保护,A装置中,金属铁做原电池的负极,更易被腐蚀,在C装置中,金属铁和水以及少量的氧气接触,也会被腐蚀,故答案为:BD;
(2)①在铁件的表面镀铜的电镀池中,作阳极的是镀层金属铜,故答案为:铜;
②在铁件的表面镀铜的电镀池中,做阴极的是待镀金属铁,该极上金属阳离子铜离子发生得电子的还原反应,即Cu2++2e-=Cu,故答案为:Cu2++2e-=Cu;
③镀铜铁破损后,金属铁为负极,镀锌铁破损后,金属铁是正极,在原电池中,负极金属更易被腐蚀,所以镀铜铁比镀锌铁更容易被腐蚀,
故答案为:镀铜铁破损后,金属铁为负极,镀锌铁破损后,金属铁是正极,负极金属易被腐蚀.
本题解析:
本题难度:一般
5、选择题 埋在地下的自来水管,在下列情况下被腐蚀的速度最慢的是
A.在含有铁元素的较多的酸性土壤中
B.在潮湿、疏松的土壤中
C.在自来水的铁管上用导线连接一块锌片后,再埋入不透气的土壤中
D.在自来水的铁管上用导线连接一块铜片后,再埋入潮湿、疏松的土壤中
参考答案:C
本题解析:C.构成原电池,牺牲阳极,阴极保护法,负极腐蚀速率加快,正极得到保护。
本题难度:一般