1、选择题 下面是425℃时,在1升密闭容器中发生化学反应的浓度与速率变化示意图。
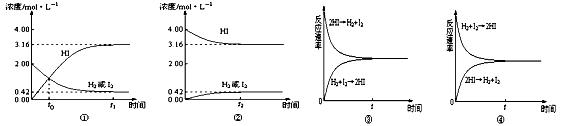
下列叙述正确的是
A.图①中to时,各组分物质的量相等,反应达到了平衡
B.图①②中当c(HI)=3.16mol/L时,反应停止了
C.图③与图④分别对应图①与②所表示的可逆反应
D.由图①②可得,化学反应的限度与建立的途径无关
参考答案:D
本题解析:略
本题难度:简单
2、选择题 下列说法不正确的是?
A.明矾净水的原理是Al3+水解产生Al(OH)3胶体,Al(OH)3胶体能吸附水中的悬浮杂质,并使之沉降
B.摩尔盐的制备原理为:6H2O+FeSO4+(NH4)2SO4=(NH4)2Fe(SO4)?6H2O,反应之所以能进行的原因是(NH4)2Fe(SO4)?6H2O溶解度最小
C.镀锌铁皮在酸中溶解,当镀层反应完全时,产生氢气的速率会突然减慢
D.将火柴头直接浸入品红溶液中,可以检验火柴头中是否含有硫元素
参考答案:D
本题解析:
答案:D
A.正确,明矾净水的原理是Al3+水解产生Al(OH)3胶体,Al3++3H2O Al(OH)3+3H+ ,Al(OH)3胶体能吸附水中的悬浮杂质,并使之沉降
Al(OH)3+3H+ ,Al(OH)3胶体能吸附水中的悬浮杂质,并使之沉降
B.正确,摩尔盐的制备原理为:6H2O+FeSO4+(NH4)2SO4=(NH4)2Fe(SO4)?6H2O,反应之所以能进行的原因是(NH4)2Fe(SO4)?6H2O溶解度最小,达到饱和后能从溶液中析出。
C.正确,镀锌铁皮在酸中溶解,当镀层反应完全时,不再形成原电池,反应速率变慢,产生氢气的速率会突然减慢
D.不正确,将火柴头直接浸入品红溶液中,无法检验火柴头中是否含有硫元素,可将它燃烧后,将生成的气体通入品红溶液。
本题难度:一般
3、选择题 在一定温度下,可逆反应N2(g)+3H2(g)?2NH3(g)达到平衡状态的标志是( )
A.氨气生成的速率与氮气分解的速率相等?
B.氮气、氢气、氨气的浓度不再变化?
C.单位时间内,生成n?mol?氮气,同时生成3n?mol?氢气?
D.氮气、氢气、氨气分子数之比为1:3:2?
参考答案:A.当氨气的生成速率与氮气的生成速率之比为2:1时,该反应达到平衡状态,当氨气的生成的速率与氮气分解的速率相等时该反应未达到平衡状态,故A错误;
B.当反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,所以当氮气和氢气、氨气浓度不再变化时,该反应达到平衡状态,故B正确;
C.无论该反应是否达到平衡状态,单位时间内,生成n?mol?氮气,就同时生成3n?mol?氢气,所以该反应不一定达到平衡状态,故C错误;
D.当氮气、氢气、氨气分子数之比为1:3:2时,该反应可能达到平衡状态,也可能没有达到平衡状态,与反应物初始浓度、转化率有关,故D错误;
故选B.
本题解析:
本题难度:简单
4、选择题 对于在一密闭容器中进行的下列反应:C(s)+ O2(g) CO2(g)下列说法中错误的是? (? )
CO2(g)下列说法中错误的是? (? )
A.将木炭粉碎成粉末状可以加快化学反应速率
B.升高温度可以加快化学反应速率
C.把容器的体积缩小到原来的一半,各物质的物质的量不变, 化学反应速率不变
D.增加木炭的量可以加快化学反应速率
参考答案:CD
本题解析:木炭是固体,改变固体的表面积可以加快反应速率,A正确;同样升高温度反应速率是加快的,B正确;把容器的体积缩小到原来的一半,即增大压强,平衡不移动,但反应速率加快,C不正确;改变固体的质量,反应速率不变,D不正确,答案选CD。
点评:浓度对反应速率和平衡状态的影响不能适用于固体和纯液体;压强对反应速率或平衡状态的影响只能适用于有气体参加或生成的,且实质是通过改变浓度引起的。
本题难度:一般
5、填空题 (一)、将2 mol SO2和1 mol O2气体在1L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2 (g) 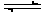 ?2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L。试计算:(1)O2的化学反应速率V(O2)=?; (2)2s时的O2浓度?。
?2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L。试计算:(1)O2的化学反应速率V(O2)=?; (2)2s时的O2浓度?。
(二)、某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如下图所示。
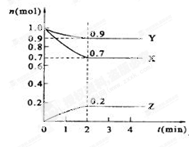
(1)X的转化率是?
(2)由图中所给数据进行分析,该反应的化学方程式为?;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=?;
(4)当反应进行到第?min,该反应达到平衡。
参考答案:(1) υ(O2)="0" .15mol/(L・s)? c(O2)=0.7? mol/L
(2) 30%? 3X+Y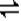 2Z? 0.05mol/(l.・min)? 2
2Z? 0.05mol/(l.・min)? 2
本题解析:(一) 2s后测得SO3的浓度为0.6 mol/ L,所以V(O2)="0.5" V(SO2)=0.5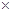 0.6/2=0 .15mol/(L・s),2s时的O2浓度=1-0 .15
0.6/2=0 .15mol/(L・s),2s时的O2浓度=1-0 .15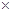 2=0.7 mol/L;
2=0.7 mol/L;
(二)由图可以知道,每反应0.1molY,和0.3molX就生成了0.2mol的Z,所以其反应的化学方程式为3X+Y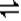 2Z,? X的转化率=0.3/1
2Z,? X的转化率=0.3/1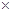 100%=30%,(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=0.2/2/2= 0.05mol/(l.・min);(4)由图可以看出,当反应时间为2min时,各物质的浓度均不再变化,所以当反应进行到第2min,该反应达到平衡。
100%=30%,(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=0.2/2/2= 0.05mol/(l.・min);(4)由图可以看出,当反应时间为2min时,各物质的浓度均不再变化,所以当反应进行到第2min,该反应达到平衡。
点评:本题考查了化学平衡,反应速率的相关计算,是高考考查的重点,该题综合性强,但难度不大。
本题难度:一般