1、选择题 热化学方程式C(s)+H2O(g)
?CO(g)+H2(g);△H=+131.3kJ/mol表示( )
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
参考答案:C
本题解析:
本题难度:简单
2、选择题 在同温同压下,下列各组热化学方程式中,Q1>Q2的是
A.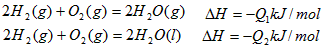
B.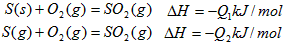
C.
D.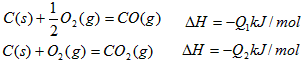
参考答案:C
本题解析:
本题难度:一般
3、选择题 1 g氢气在氧气中燃烧生成液态水,放出142.9 kJ热量,表示该反应的热化学方程式的是
[? ]
A.H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ/mol
B.H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8 kJ/mol
C.2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ/mol
D.H2(g)+1/2O2(g)=H2O ΔH=-285.8 kJ/mol
参考答案:A
本题解析:
本题难度:简单
4、填空题 (14分)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上常用CO和H2反应生产CH3OH,并开发出甲醇燃料电池。
(1)已知:CO(g)+1/2O2(g)=CO2(g) △H=-283.0 kJ・mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H=-1453.0 kJ・mol-1
则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为 。
(2)工业上常利用反应CO(g)+2H2(g) CH3OH(g) △H<0合成甲醇,在230℃~270℃最为有利。为研究合成气最合适的起始组成比,分别在230℃、250℃和270℃进行实验,结果如图。
CH3OH(g) △H<0合成甲醇,在230℃~270℃最为有利。为研究合成气最合适的起始组成比,分别在230℃、250℃和270℃进行实验,结果如图。
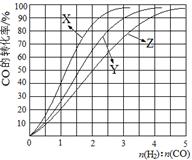
230℃的实验结果所对应的曲线是 (填字母);该温度下工业生产适宜采用的合成气组成n(H2):n(CO) 的比值范围是 (填字母) 。
A.1~1.5 B.2.5~3 C.3.5~4.5
(3)制甲醇所需要的氢气,可用下列反应制取:H2O(g)+CO(g) H2(g)+CO2(g) △H<0,某温度下该反应的平衡常数K=1。试回答下列问题:
H2(g)+CO2(g) △H<0,某温度下该反应的平衡常数K=1。试回答下列问题:
①该温度下,若起始时c(CO)="1" mol・L-1,c(H2O)="2" mol・L-1,反应进行一段时间后,测得H2的浓度为0.5 mol・L-1,则此时该反应v(正) v(逆)(填“>”、“<”或“=”)。
②若降低温度,该反应的K值将 (填“增大”、“减小”或“不变”)。
(4)某实验小组设计了如图所示的甲醇燃料电池装置。
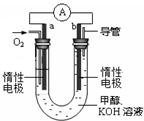
①该电池工作时,OH-向 极移动(填“a”或“b”)。
②工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为 。
参考答案:(每空2分,共14分)(1)CH3OH(l)+ O2(g) = CO(g) + 2H2O(l) ΔH=―443.5 kJ
本题解析:
本题难度:困难
5、填空题 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ・mol―1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ・mol―1
则甲烷直接将NO2还原为N2的热化学方程为 。
(2)降低汽车尾气的方法之一是在排气管上安装催化 转化器,发生如下反应:
2NO(g)+2CO(g)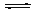 N2(g)+2CO2(g) △H<0。
N2(g)+2CO2(g) △H<0。
若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K= 。
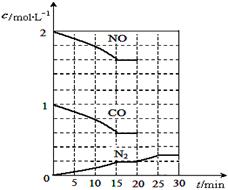
若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将 移动(填“向左”、 “向右”或“不”)。
20min时,若改变反应条件,导致N2浓度发生如上图所示的变化,则改变的条件可能是 (填序号)。
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(3)肼(N2H4)用亚硝酸(HNO2)氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977。写出肼与亚硝酸反应的化学方程式 。
参考答案:(1)CH4(g)+2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867kJ・mol-1(2分)
(2)k=" 5/144" 或0.0347 (2分); 不(1分); ② (1分)
(3) N2H4 +HNO2==HN3 + 2H2O(2分)
本题解析:(1)根据盖斯定律,甲烷直接将NO2还原为N2的?H=1/2?H1+1/2?H2=-867kJ・mol-1,所以热化学方程式为:CH4(g)+2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867kJ・mol-1
(2)根据图中所示浓度可知c(CO2)=0.4mol/L,则
K=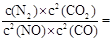
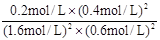 =
=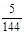
再向容器中充入CO、N2各0.6mol, Q仍为 5/144,所以平衡不移动;20min时,从图中看出平衡正向移动,N2起始浓度没变,所以选②。
(3) 根据氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,可求得分子式为HN3,该反应的化学方程式为:N2H4 +HNO2==HN3 + 2H2O
考点:本题考查热化学方程式的书写、平衡常数、平衡移动、化学方程式的书写。
本题难度:困难