1、填空题 二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为:3H2(g) +3CO(g)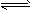 CH3OCH3(g)+CO2(g) △H=- 246.4 kJ/mol 它可以分为两步,反应分别如下:①4H2(g)+2CO(g)=CH3OCH3(g)+H2O(g) △H1=-205.1 kJ/mol;
CH3OCH3(g)+CO2(g) △H=- 246.4 kJ/mol 它可以分为两步,反应分别如下:①4H2(g)+2CO(g)=CH3OCH3(g)+H2O(g) △H1=-205.1 kJ/mol;
②CO(g) +H2O(g)=CO2(g) +H2(g) △H2=____________
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速率和CO转化率的 是____(填字母代号)。
a.降低温度 b.加入催化剂 c.缩小容器体积 d.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入3 mol H2、3 mol CO、1 mol CH3OCH3、1 mol CO2,在一定温度和压强下发生反应:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:
CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:
①反应开始时正、逆反应速率的大小:v(正)_____ (填“>”、“<”或“=”)v(逆)。
②平衡时n(CH3OCH3)=_________,平衡时CO的转化率=_________。
参考答案:(1)-41.3 kJ/mol
(2)cd
(3)①>;②1.75mol;75%
本题解析:
本题难度:一般
2、选择题 下列说法不正确的是( )
A.已知4HC1(g)+O2(g)=2H2O(g)+2C12(g)能自发进行,则该反应:△H<0,△S<0
B.常温下0.1mol?L-1CH3COOH的pH为2.88,可以说明CH3COOH为弱电解质
C.其他条件不变,增大压强,平衡可能移动,但平衡常数一定不变
D.铁制品的表面镶锌块和铁制品表面镀锡,都能起到防腐的作用,且防腐原理是相同的
参考答案:A.生成气体的物质的量减小,则△S<0,反应能自发,应满足△G=△H-T?△S<0,则△H<0,故A正确;
B.0.1mol?L-1CH3COOH的pH为2.88,说明醋酸没有完全电离,为弱电解质,故B正确;
C.平衡常数为温度的函数,只与温度有关,与压强无关,故C正确;
D.铁制品的表面镶锌块,锌为负极,铁制品表面镀锡,可起到隔绝空气的作用,二者防护的原理不同,故D错误.
故选D.
本题解析:
本题难度:一般
3、选择题 对苯二酚是摄影业中常用显影剂,它在水中电离出的阴离子对已曝光的AgBr 有显影作用,有关变化可表示为: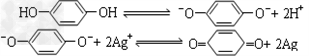 ,能使显影速度明显加快的添加剂是?
,能使显影速度明显加快的添加剂是?
[? ]
A.KBr?
B.Na2CO3
C.CH3COOH
D.H2O
参考答案:B
本题解析:
本题难度:一般
4、选择题 某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)?
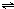
2C(g)达到平衡时,测得A、B、C物质的量之比为2:2:1.若保持温度不变,以2:2:1的物质的量之比再充入A、B、C,下列判断正确的是( )
A.平衡向逆反应方向移动
B.平衡不会发生移动
C.C的质量分数增大
D.C的质量分数可能减小
参考答案:A、达到平衡,此时测得n(A):n(B):n(C)=2:2:1,若保持温度不变,以n(A):n(B):n(C)=2:2:1的比例向该容器中再充入A、B和C,相当于在原来的基础上缩小体积,增大压强,反应前气体的化学计量数之和大于生成物的气体化学计量数之和,则增大压强,平衡向正反应方向移动,故A错误;
B、根据A知化学平衡会向正反应方向移动,故B错误;
C、化学平衡会向正反应方向移动,所以C的质量分数增大,故C正确;
D、化学平衡会向正反应方向移动,C的质量分数增大,故D错误.
故选C.
本题解析:
本题难度:一般
5、填空题 将各2a mol的P、Q、R、S在一密闭容器中混合,发生如下反应:xP+yQ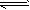 zR+wS。达到平衡后,测得n(P)=a mol,n(Q)=
zR+wS。达到平衡后,测得n(P)=a mol,n(Q)=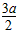 mol,n(R)=
mol,n(R)= mol,n(S)=3a mol,已知四种物质中只有R是固体。
mol,n(S)=3a mol,已知四种物质中只有R是固体。
(1)若该反应中物质的化学计量数x=2,则z=________,w=________。
(2)达到平衡时,P的转化率是____________。
(3)如果只改变压强,化学反应速率发生变化,但化学平衡不移动。则该反应中各物质的聚集状态分别是:Q____________,S____________。
(4)如果只升高温度,反应一段时间后,各物质的物质的量均变为2a mol,则该反应的正反应为________热反应。
参考答案:(1)3;2
(2)50%
(3)液态;气态
(4)放
本题解析:
本题难度:一般