1、实验题 实验室获取氮气有很多种途径,常见的3种方法是:
方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气。
进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
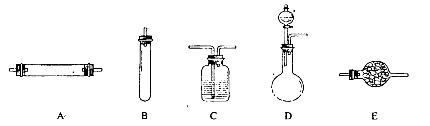
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用_____________________(选填装置编号)。请写出生石灰在此反应中的两个作用:__________________________________,___________________________________________.
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置_________________
(选填装置编号)中加入_________________________以除去其它杂质气体。
(3)方法三:制氮气的化学方程式为:_____________________________________________。
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂。在制取氮气的3种方法中,联合使用方法―和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:_____________
______________________________________________________________________________.
(5) 1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大5‰左右。若上述实验设计与操作均无错误,且氮气已完全干燥,
请解释产生这一现象的原因:_______________________________________________.
参考答案:(1)D; CaO和水反应,减少了溶剂;CaO和水反应放热,降低了氨气的溶解度。
(2)E?碱石灰
(3)NaNO2+NH4Cl NaCl+N2↑+2H2O;
NaCl+N2↑+2H2O;
(4)Cu和CuO可以循环使用,节省试剂;避免使用有毒物质NaNO2而造成污染,
(5)方法二制的氮气含有稀有气体的密度比氮气密度大,所以导致氮气密度偏大
本题解析:(1)用CaO和浓氨水反应,应选固液常温型的发生装置,即D;浓氨水常温下跟生石灰反应生成氨气和氢氧化钙,化学方程式为CaO+NH3?H2O=NH3↑+Ca(OH)2,因为氨水不稳定易挥发,生石灰和水反应生成熟石灰的过程中,生石灰的两个作用是:一方面消耗氨水溶液中的水,另一方面放出的热量促使氨水挥发、分解而得到氨气;
(2)空气中除了氮气、氧气外,还含有二氧化碳、水蒸气等,为保证所得氨气尽可能纯净,要除去空气中多余的水蒸气、二氧化碳等杂质,可以通过碱性干燥剂-碱石灰,既可以吸收二氧化碳又能吸收水;
(3)根据信息反应物是亚硝酸钠(NaNO2)和氯化铵,反应条件是加热,氮元素全部转化为氮气,反应前后元素的种类不变,因此生成物还有氯化钠和水,因此反应的方程式为:
NaNO2+NH4Cl NaCl+N2↑+2H2O;
NaCl+N2↑+2H2O;
(4)从题中信息可知,NH3和CuO生成Cu和N2而空气和Cu生成CuO,故Cu和CuO可以循环使用,方法三使用有毒的亚硝酸钠,方法一和二避免使用有毒物质而造成污染,因此联合使用方法一和方法二与单独使用方法三相比的优点有:铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染).
(5)将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末只是除去了氧气,其中还含有稀有气体等杂质,由于稀有气体的密度比氮气密度大,所以导致氮气密度总是偏大5‰左右;
本题难度:一般
2、实验题 用浓度为0.10 mol/L的KMnO4(H+)溶液滴定未知浓度的H2C2O4(弱酸)溶液,其实验步骤如下:
I、滴定前的准备:
?①?→ 用蒸馏水清洗 → 用待装溶液润洗 → 装液→ ?②??→ 调节液面在零刻度或零刻度以下 → 记录初始读数
II、滴定:
分别取20.00 mL 草酸溶液于4个洁净的锥形瓶中,滴加几滴MnSO4溶液,然后用标准的KMnO4(H+)溶液进行滴定至终点,记录最终读数。数据如下:
测定次序
| 第一次
| 第二次
| 第三次
| 第四次
|
初始读数(mL)
| 0.40
| 0.10
| 0.90
| 0.00
|
最终读数(mL)
| 25.05
| 20.10
| 21.00
| 19.90
|
V标(mL)
| 24.65
| 20.00
| 20.10
| 19.90
|
III、实验数据处理:略
请回答下列问题:
(1)将步骤I中的操作补充完整:
①__________________________?
②__________________________
(2)KMnO4(H+)溶液应装入________式滴定管进行滴定;
(3)向锥形瓶中滴加MnSO4溶液的作用是_____________________________________;判断已达滴定终点的现象是:_____________________________________;
(4)该滴定反应的离子方程式为:__________________________________________;
(5)实验测得草酸溶液的浓度为_____________mol/L;
(6)下列操作会引起实验结果偏高的是_____________
A.向锥形瓶中加入了较多 MnSO4溶液
B.滴定振摇时,锥形瓶中溶液溅出
C.滴定时,锥形瓶内壁附有紫红色溶液,未用蒸馏水冲洗
D.滴定结束时,仰视读数
参考答案:(13分)
(1)①查漏;?②排除滴定管尖嘴处的气泡?(各1分)
(2)酸(1分)
(3)作反应催化剂,加快KMnO4氧化H2C2O4的速率;
溶液由无色变为(紫)红色,半分钟不褪色? (各2分)
(4) 2MnO4― +? 5H2C2O4 +? 6H+ ="=" 2Mn2+ + 10CO2 ↑+ 8H2O?(2分)
(5) 0.25 (2分)
(6) CD?(2分)
本题解析:(1)滴定实验开始就检查滴定管是否合格,为检漏操作,待装液以后要排气泡。(2)KMnO4(H+)溶液具有很强的氧化性,装到酸式滴定管中。(3)MnSO4溶液做为催化剂加快反应速率。(6)A项:无影响;B项:会偏低。
点评:本题考查的是滴定实验操作,学生要注意滴定实验中操作的顺序以及规范操作,且能对有误差能进行分析出来。
本题难度:一般
3、选择题 实验室欲快速制取氢气,应采取的措施是
A.用纯锌和稀硫酸反应
B.用含铜等的粗锌和稀硫酸反应
C.用纯锌和浓硫酸反应
D.用含铜等的粗锌和稀硝酸反应
参考答案:B
本题解析:A 错误,纯锌和稀硫酸反应较慢。
B 正确,含铜等的粗锌和稀硫酸时,会形成铜锌原电池,加快反应速率
C 错误,纯锌和浓硫酸反应不生成氢气,产生的是二氧化硫气体。
D 错误,含铜等的粗锌和稀硝酸反应也不生成氢气,生成的是二氧化氮气体
本题难度:一般
4、实验题 .某化学兴趣小组测定某FeCl3样品(只含少量FeCl2杂质)中铁元素的质量分数,按以下实验步骤进行操作:
① 称取a g样品,置于烧杯中;
② 加入适量盐酸和蒸馏水,使样品溶解,然后准确配制成250.00mL溶液;
③量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;
④ 加入过量氨水,充分搅拌,使沉淀完全;
⑤ 过滤,洗涤沉淀;
⑥ 将沉淀转移到某容器内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;
⑦……。

请根据上面叙述,回答:
(1)上图所示仪器中,本实验步骤①②③中必须用到的仪器是E和?(填字母)。?
(2)写出步骤④中发生反应的离子方程式?。
(3)样品中的杂质Fe2+有较强的还原性,完成并配平下列反应的离子方程式
Fe2+? +? ClO3― +??= ?Fe3+?+? Cl― +? H2O
从理论上分析,上述实验中若将氯水改为NaClO3时,对实验结果造成?(填偏大、偏小或不影响),
(4)若容器质量是W1 g,最终容器和固体的总质量是W2 g,则样品中铁元素的质量分数为?。(列出算式,不需化简)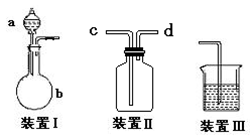
参考答案:(1)C F G?
(2)Fe3+ +3NH3H2O=Fe(OH)3↓+ 3 NH4+?
(3)6Fe2+? +? ClO3― + ?6 H+= 6Fe3+?+? Cl― + 3H2O ,无影响,

本题解析:(1)实验步骤①是称量需要用到天平F,步骤②溶解并配制溶液需要用到容量瓶G,步骤③是取一定量的溶液,由于该溶液呈酸性且Fe3+具有氧化性所以要用酸式滴定管C。
(2)步骤④是向的溶液中Fe3+加入碱性的氨水,Fe3+会与碱反应生成Fe(OH)3,反应的离子反应方程式为Fe3+ +3NH3H2O=Fe(OH)3 ↓+ 3 NH4+
(3)根据氧化还原反应中得失电子守恒,先配平电子,然后根据电荷守恒确定空格中为氢离子,并配平,结果为6Fe2+? +? ClO3― + ?6 H+= 6Fe3+?+? Cl― + 3H2O;由于最后称量的是Fe2O3这一步只是将Fe2+氧化为Fe3+,只要能够实现该转化并且不对后面的沉淀产生影响都是可以的,所以若将氯水改为NaClO3时,对实验结果无影响。
(4)容器中剩余的固体为Fe2O3,并且Fe2O3的质量为(W2- W1)g,根据铁元素的质量分数计算铁元素的质量为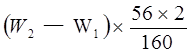 g,又这些铁元素只是25.00mL溶液中的铁元素质量,则250mL溶液中铁元素可以计算出来,在除以样品总质量即为铁元素的质量分数,为:
g,又这些铁元素只是25.00mL溶液中的铁元素质量,则250mL溶液中铁元素可以计算出来,在除以样品总质量即为铁元素的质量分数,为:
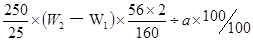
本题难度:一般
5、选择题 下列关于层析实验的说法正确的是:
A.点样后应在滤纸上形成一个直径较大的样斑,便于实验时观察
B.展开剂可以既是流动相又是固定相
C.为使层析实验有较好的分离效果,试样溶液浓度应较小
D.纸层析法简称纸层析,是色谱分析法的一种
参考答案:D
本题解析:A不正确,点样的目的是对照试验。展开剂可以只能是流动相,B不正确。流动相溶剂对分离物质有适当的溶解度,太大或太小均是错误的。所以正确的答案选D。
本题难度:简单