1、填空题 (1)铜是人类最早使用的金属之一,以下是冶炼铜的一个反应:
Cu2S+2Cu2O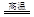 6Cu+SO2
6Cu+SO2
该反应中被氧化的元素是?,若反应中转移1mol电子,得到Cu?mol。?
(2)下列两种方法均可以制备CuSO4。
方法一:2Cu+O2 2CuO,CuO+H2SO4=CuSO4+H2O
2CuO,CuO+H2SO4=CuSO4+H2O
方法二:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
①假如某工厂欲生产CuSO4,请选择一种方法,并说明理由:?
?。
②有同学认为,生成等量的硫酸铜两种方法消耗的能量相同,因为反应都是铜转变为CuSO4,你认为上述说法?(填“正确”或“不正确”),原因是?
?。
2、选择题 下列叙述正确的是
A.将FeCl3溶液加热蒸干得到FeCl3固体
B.向Fe(NO3)2溶液中加少量盐酸,无明显现象
C.向氢氧化镁悬浊液中滴加FeCl3溶液,无明显现象
D.向FeSO4溶液中滴加NaOH溶液,先出现白色沉淀,最终沉淀转化成红褐色
3、选择题 对I~IV的实验操作现象判断正确的是
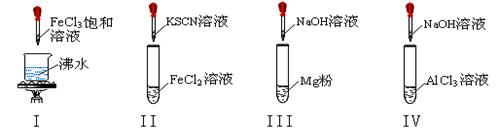
A.实验I:产生红褐色沉淀
B.实验II:溶液颜色变红
C.实验III:放出大量气体
D.实验IV:先出现白色沉淀,后溶解
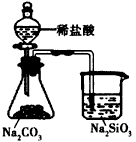
4、选择题 下列关于一些元素化合物的性质叙述正确的是
[? ]
A.硝酸工业中NO可循环利用,理论上1 mol氨气可生成2/3 mol硝酸
B.1 mol Na在化学反应中失去的电子比1 mol Al少,但Na的金属性却强于Al的金属性
C.由于铝在常温下不能与氧气反应,所以铝制品具有一定的抗腐蚀性能,是一种应用广泛的金属材料
D.上图中若锥形瓶中有气体产生,烧杯中液体变浑浊,则可说明非金属性:Cl>C> Si
5、选择题 下列有关实验的现象或反应,与原理解释符合因果关系的是(?)
?
| 现象或反应
| 原理解释
|
A
| 铝箔在酒精灯火焰上加热熔化但不滴落
| 铝的金属性不活泼,不能与氧气反应
|
B
| 硫与氧气只有在加热条件下才能进行反应
| 该反应为吸热反应
|
C
| 向碳酸钠和氢氧化钠溶液中滴加酚酞,溶液都呈红色
| 碳酸钠和氢氧化钠都是碱
|
D
| 常温下,铝制容器可用于盛装冷的浓硫酸
| 常温下,铝遇冷的浓硫酸发生钝化
|
?