1���ƶ��� ��֪A����;��㷺�Ľ������ʣ�B�dz����³�Һ̬�Ļ����E��һ�ֻ���ɫ�����塣��ͼ�в��ֲ���δ�������?
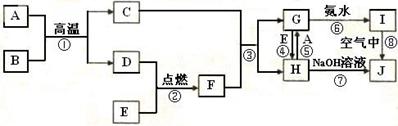
�ش��������⣺
(1)д��C�Ļ�ѧʽ?��д����Ӧ�ٵĻ�ѧ��Ӧ����ʽ��?��
(2)д����Ӧ�۵����ӷ���ʽ?
д����Ӧ�ܵ����ӷ���ʽ________________________________________
(3)����G��Һ�������ӵķ��� ?��
(4)��H��Һ�μӵ���ˮ�У�����������У��õ�����Һ��ɫΪ_________
��ɢ�ʵĴ�С��___________________.
�ο��𰸣���ÿ�ո�2�֣���14�֣���1��Fe3O4? 3Fe��4H2O(g) Fe3O4��4H2��
Fe3O4��4H2��
(2)F3O4��8H��=2Fe3����Fe2����4H2O? 2Fe2����Cl2=2Fe3��2Cl��
(3)�ȼ����軯����Һ��û�������ټ���ˮ����Һ��졣��Ҳ��д������������Һ��
(4)���ɫ? 1nm----100nm
���������A����;��㷺�Ľ������ʣ���A������B�dz����³�Һ̬�Ļ�������ڸ������ܺ�����Ӧ������B��ˮ��E��һ�ֻ���ɫ�����壬��E�����������ڸ����º�ˮ������Ӧ��������������������������D�������ɷ�Ӧ����˵��D��������C��������������F���Ȼ��⣬����ˮ���õ����ᡣ�����������������Ӧ�����Ȼ������Ȼ�������H�ܺ�����Ӧ����G������H���Ȼ�����G���Ȼ���������I��������������J������������
�����������Ǹ߿��еij������ͣ����ڻ���������Ŀ��顣�����������У�����֪ʶ�����ض�ѧ������֪ʶ�Ĺ��̸�ѵ��������������Ҫע����ǻ�ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȡ�
�����Ѷȣ�һ��
2������� �±�ΪԪ�����ڱ���һ���֣������Ԫ�آ�һ���ڱ��е�λ�ã��û�ѧ����ش��������⣺
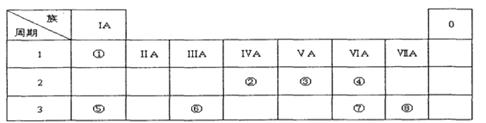
��1���뻭��Ԫ�آ�������ӽṹʾ��ͼ?��
��2���ܡ��ݡ��ߵ�ԭ�Ӱ뾶��С�����˳��Ϊ?��
��3���ݺ͢�����������Ӧˮ����ļ���ǿ��Ϊ?>?��
��4���ܡ�������Ԫ�ص�ԭ�Ӱ�1:1��ɵij���������ĵ���ʽΪ?��
���ɱ��Т�һ���е�һ�ֻ���Ԫ���γɵij�������A��B��C�ɷ������·�Ӧ������������ȥ�����Իش�
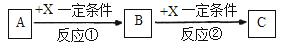
��1����X��һ�ֳ������ɽ������ʣ���C��ˮ��Һ�еμ�AgNO3��Һ������������ϡHNO3�İ�ɫ�����������C��Һ�н������ӵķ�����?����֪��������Һ�иý��������ܱ�˫��ˮ������д���÷�Ӧ�����ӷ���ʽ?��
��2����A��B��CΪ����ͬһ����Ԫ�ص��������XΪǿ����ʣ�A��Һ��C��Һ��Ӧ����B����B�Ļ�ѧʽΪ?��д��A��C����Һ��Ӧ�����ӷ���ʽ____?��
�ο��𰸣���1��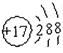 ��1�֣�
��1�֣�
��2��Na>S>O ��2�֣�
��3�� NaOH >Al(OH)3?��2�֣�
��4��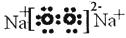 ��2�֣�
��2�֣�
��1���ȼ���KSCN��Һ���Ժ�ɫ���ټ�����ˮ�Ժ�ɫ�������������������Һ��������ɫ������Ȼ���ɻ���ɫ������ɺ��ɫ��������2�֣� H2O2+2Fe2++2H+=2Fe3++2H2O ��2�֣�
��2��Al(OH)3 ��1�֣��� Al3++3AlO2-+6H2O=4Al(OH)3����2�֣�
�������������Ԫ�������ڱ��е�λ�ÿ�֪����ΪH����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪS����ΪCl����1����ΪCl�������ӵĽṹʾ��ͼΪ ����2������ԭ�Ӱ뾶�Ƚ�ԭ���Ӳ�Խ�࣬�뾶Խ��ͬ���ڴ�������ԭ�Ӱ뾶�ڼ�С��ԭ�Ӱ뾶ΪNa��S��O����3����ΪNa����ΪAl��������Na��Al��������������ˮ����ļ���ΪNaOH >Al(OH)3����4���ܡ�������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���������ΪNa2O2�������ʽΪ
����2������ԭ�Ӱ뾶�Ƚ�ԭ���Ӳ�Խ�࣬�뾶Խ��ͬ���ڴ�������ԭ�Ӱ뾶�ڼ�С��ԭ�Ӱ뾶ΪNa��S��O����3����ΪNa����ΪAl��������Na��Al��������������ˮ����ļ���ΪNaOH >Al(OH)3����4���ܡ�������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���������ΪNa2O2�������ʽΪ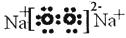 ����1����C��ˮ��Һ�еμ�AgNO3��Һ������������ϡHNO3�İ�ɫ������C�к���ClԪ�أ�X��һ�ֳ������ɽ������ʣ���XΪ����AΪ������BΪ�Ȼ�����CΪ�Ȼ�������C�е�������Ϊ�������ӣ������������ӵIJ���Ϊ�ȵμ�KSCN��Һ���Ժ�ɫ���ټ�����ˮ�Ժ�ɫ������NaOH��Һ���Ȳ�����ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ������������Һ�����������ܱ�˫��ˮ���������ӷ�ӦΪH2O2+2Fe2++2H+�T2Fe2++2H2O����2����A��B��CΪ����ͬһ����Ԫ�ص��������XΪǿ����ʣ�A��Һ��C��Һ��Ӧ����B����ת����ϵ��֪��AΪ���������Σ�BΪAl��OH��3��CΪƫ�����Σ�XΪ�������ƣ�����AΪƫ�����Σ�BΪAl��OH��3��CΪ���������Σ�XΪ���ᣩ����A��C��Ӧ�����ӷ�ӦΪ
����1����C��ˮ��Һ�еμ�AgNO3��Һ������������ϡHNO3�İ�ɫ������C�к���ClԪ�أ�X��һ�ֳ������ɽ������ʣ���XΪ����AΪ������BΪ�Ȼ�����CΪ�Ȼ�������C�е�������Ϊ�������ӣ������������ӵIJ���Ϊ�ȵμ�KSCN��Һ���Ժ�ɫ���ټ�����ˮ�Ժ�ɫ������NaOH��Һ���Ȳ�����ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ������������Һ�����������ܱ�˫��ˮ���������ӷ�ӦΪH2O2+2Fe2++2H+�T2Fe2++2H2O����2����A��B��CΪ����ͬһ����Ԫ�ص��������XΪǿ����ʣ�A��Һ��C��Һ��Ӧ����B����ת����ϵ��֪��AΪ���������Σ�BΪAl��OH��3��CΪƫ�����Σ�XΪ�������ƣ�����AΪƫ�����Σ�BΪAl��OH��3��CΪ���������Σ�XΪ���ᣩ����A��C��Ӧ�����ӷ�ӦΪ
Al3++3AlO2-+6H2O�T4Al��OH��3����
�����Ѷȣ�����
3������� ��16�֣���A��B��C���ֶ�����Ԫ�������ڱ������λ������ͼ��
��1��A��C�γɵ�Һ̬�������dz�������Ҫ�л��ܼ�����A��B��C����Ԫ������������Ӧ��ˮ����������ǿ������˳���ǣ�?>?>??���û�ѧʽ��ʾ����
��2��X��YΪB��C����Ԫ���γɵĵ��ʡ���״���£�X���ܶ�Ϊ3��17g/L��Z��һ�ֻ������ɫ��Ӧ����ɫ�����ܲ�������������0��1mol/LZˮ��ҺpH=13��X��Y��Z����ͼת����ϵ��
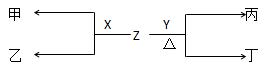
��д��X��Z��Ӧ������ ����ʽ��?��
����ʽ��?��
����֪������ϡ���ᷴӦ����ʹƷ����ɫ�����塣���ĵ���ʽ?������ˮ��ҺpH?7������ڡ���С�ڡ����ڡ�������ԭ��Ϊ
?�������ӷ���ʽ��ʾ����
�۽�20mL0��5mol/L����Һ��μ���20mL0��2mol/LKMnO4��Һ�������ữ���У�ǡ����ɫ��д����Ӧ�����ӷ���ʽ?��
��д��X��ˮ��Ӧ����������ĵ���ʽ?��?��
�ο��𰸣�
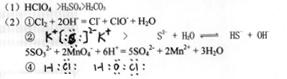
�����������
�����Ѷȣ�һ��
4������� ������ѧij��ѧ��ȤС���������⣨Fe2O3������ϵ��ʵ�飬���ʼ��ϵͼ���£�������ѧ֪ʶ�ش�������⣺

��1��д��A��B��C�������ʵ����ƣ�A______?B______?C______
��2��д����A�����ˮ���Ʊ�B�����ӷ���ʽ��______��
��3����ȤС�������˶���ʹBת��ΪC�ķ�������д������Ϊ���е�һ�ַ�����______��
��4������˵����ȷ���У�����ţ���______��
��Bת��ΪC�Ĺ��̷����˻�ѧ��Ӧ
����A�Ʊ�Bʱ������Խ��Խ��
������B���ж����ЧӦ
�ܰ�B��C�Ļ������ˣ���Һ��ɫ��
������ϵ�з�Ӧ�������漰������ԭ��Ӧ��
�ο��𰸣���1�����⣨Fe2O3�������������ᷴӦ���ɵ�AΪ�Ȼ������Ȼ��������ˮ�л���B�����������壬�Ȼ������������Ʒ�Ӧ������C���������������ʴ�Ϊ���Ȼ�����Һ�������������壻��������������
��2�����Ȼ��������ˮ���Ʊ������������壬ԭ���ǣ�Fe3++3H2O?��?.?Fe��OH��3�����壩+3H+���ʴ�Ϊ��Fe3++3H2O?��?.?Fe��OH��3�����壩+3H+��
��3������۳������������Ȼ���ҽ����Ӳ���Fe��OH��3��Ӧ��ǿ����ʵȣ��ʴ�Ϊ�����Ȼ���ҽ����Ӳ���Fe��OH��3��Ӧ��ǿ����ʣ�дһ�ּ��ɣ���
��4���ٽ���ľ۳��������仯���̣����Ԣٴ���
�ڽ��Ȼ��������ˮ���Ʊ�������������ʱ������ʱ�������ʹ����۳������ܳ�ʱ����ȣ��ʢڴ���
������������������ж����ЧӦ���ʢ���ȷ��
�ܰ�����������������������������ˣ�������ͨ����ֽ���ʢܴ���
��������Ӧ����û��Ԫ�ػ��ϼ۵ı仯����������ԭ��Ӧ���ʢ���ȷ��
��ѡ�ۢݣ�
���������
�����Ѷȣ���
5������� A��B��C��D��E�ֱ����5������ÿ�����ж�����18�����ӣ�����A��C�����ɵ�ԭ���γɵ������ӣ�B��D��E���Ƿ��ӣ���֪��ˮ��Һ��A��B��Ӧ������C��D��E����ǿ�����ԣ���ش�
��1���û�ѧ���ű�ʾ����5������
A______��B______��C______��D______��E______��
��2����ˮ��Һ��A��B��Ӧ�����ӷ���ʽ�ǣ�______��
�ο��𰸣���1�����к���18�����ӵ�������S2-��Cl-�������У�HCl��H2S��PH3��SiH4��F2��H2O2�ȣ���֪E����ǿ�����ԣ���EӦΪF2����֪��ˮ��Һ��A��B��Ӧ������C��D�������������ʵ����ʿ��ƶ�AΪS2-��BΪHCl��CΪCl-��DΪH2S���ʴ�Ϊ��S2-��HCl��Cl-��H2S��F2��
��2��H2SΪ���ᣬS2����HCl��Ӧ����H2S���ʴ�Ϊ��S2-+2H+=H2S����
���������
�����Ѷȣ�һ��