1、选择题 下列设备工作时,将化学能转化为电能的是(? )

2、填空题 (共12分)(1)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出257.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
①反应的热化学方程式为?。
②又已知H2O(l)=H2O(g)? ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是?kJ。
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是?。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g)?△H=―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)?△H=―47.4kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g)?△H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
_________________?
3、选择题 热化学方程式C(s)+H2O(g) CO(g)+H2(g) ΔH="+131.3" kJ・mol-1表示的
CO(g)+H2(g) ΔH="+131.3" kJ・mol-1表示的
为( )
A.碳与水反应吸收131.3 kJ的热量
B.1 mol碳和1 mol水反应吸收131.3 kJ的热量
C.1 mol固态碳与1 mol水蒸气反应产生一氧化碳气体和氢气,吸收131.3 kJ的热量
D.固态碳和气态水各1 mol反应,放出131.3 kJ的热量
4、填空题 (4分)指出下列变化能量是怎样转化的:
(1)学校燃烧煤煮饭?,
(2)给手机的电池充电?,
(3)用畜电池点亮灯泡?,
(4)电解水得到O2和H2?。
5、填空题 如图所示,把试管放入盛有25 ℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5 mL稀盐酸,试完成下列问题。
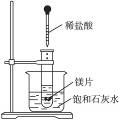
(1)实验中观察到的现象是__________________。
(2)产生上述现象的原因是__________________。
(3)写出有关反应的离子方程式__________________。
(4)由实验推知,MgCl2溶液和H2的总能量__________________(填“大于”“小于”或“等于”)镁片和盐酸的总能量。