| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《化学反应速率》高频考点强化练习(2019年最新版)(十)
 参考答案:由图可知,4~8 min期间,反应物浓度变化为(20-10)μ mol/L=10μmol/L, 本题解析: 本题难度:简单 3、选择题 一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( ) 参考答案:A、NaOH与酸中和,引起H+离子的物质的量的减小,浓度减小,氢气的总量减小,反应速率减慢,故A错误; 本题解析: 本题难度:简单 4、简答题 合成氨反应过程中的能量变化如图所示,据图回答下列问题:
A.c1<c2?B.2c1<c3?C.a1+a2=1?D.?a2<a3. 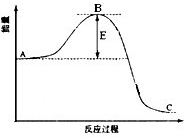 参考答案:(1)催化剂是通过降低反应的活化能来加快化学反应速率的,所以加活性铁会使图中B点降低,故答案为:降低;因为催化剂改变了反应的历程使活化能E降低; 本题解析: 本题难度:一般 5、选择题 用足量的铁片与一定量的稀硫酸反应制氢气,下列措施既能使氢气的生成速率加快,又不影响氢气的产量的是( ) |
参考答案:D
本题解析:A.滴入适量Na2SO4溶液,水对溶液起稀释作用,是化学反应速率减慢,错误;B.若不用稀硫酸,改用98%的浓硫酸,由于在浓硫酸中硫酸主要以酸分子的形式存在,H+的浓度降低,所以化学反应速率减慢,错误;C.加入少量碳酸钠固体,碳酸钠与硫酸反应消耗硫酸,使硫酸的浓度减小,速率减慢,而且由于H+的物质的量减小。所以最终氢气的量也减少,错误;D.若不用铁片,改用等质量的铁粉,由于接触面积增大,所以化学反应速率大大加快,正确。
考点:考查影响化学反应速率的因素的知识。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《化学基本理.. | |