1、选择题 已知: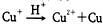 ,在NH4CuSO4中加入足量3mol/L硫酸后,下列叙述正确的是
,在NH4CuSO4中加入足量3mol/L硫酸后,下列叙述正确的是
A.有刺激性气味的氨气产生
B.若有1mol NH4CuSO4参加反应,将转移3mol e―
C.硫酸在反应中作氧化剂
D.所得溶液呈蓝色
参考答案:D
本题解析:
正确千答案:D
2NH4CuSO4+H2SO4=Cu+CuSO4+(NH4)2SO4,溶液呈蓝色,D正确,生成(NH4)2SO4,无氨气产生,A不正确;H2SO4在反应中起酸的作用,C错误。
本题难度:简单
2、实验题 分析下图装置,回答问题:
(1)装置A的烧瓶中发生的反应的化学方程式为?,?
(2)装置C的直玻管中发生的反应的化学方程式为?,
(3)在装置D的U形管中有无色晶体生成,此晶体的化学式是?,
(4)装置E中NaOH的作用是?,反应的离子方程式为?;
(5)B装置的作用很多,除了可以混匀气体外,
还可以:____________________;? __________________________________。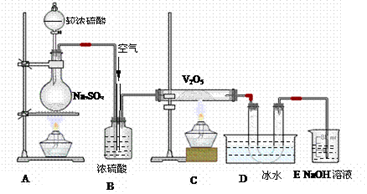
参考答案:(1)Na2SO3+H2SO4=Na2SO4+H2O+SO2,(2)2SO2+O2==2SO3,
(3)吸收尾气,SO2+2OH-=SO32-+2H2O;
(4)与圆底烧杯相接导管的气泡速度与直玻管中气泡速度之比为2:1(SO2与O2的气泡之比为2:1);干燥气体
本题解析:该实验装置图为在A产生了二氧化硫,气体在B中被干燥,然后二氧化硫和氧气在五氧化二钒催化加热下生成了三氧化硫,三氧化硫的凝固点很低,在D中被凝结,E为除去还没有反应的二氧化硫,所以(1)装置A的烧瓶中发生的反应的化学方程式为:Na2SO3+H2SO4=Na2SO4+H2O+SO2,(2)装置C的直玻管中发生的反应的化学方程式为:2SO2+O2==2SO3,(3)在装置D的U形管中有无色晶体生成,此晶体的化学式是SO3;(4)装置E中NaOH的作用是吸收尾气,其反应的离子方程式为SO2+2OH-=SO32-+2H2O;(5)B装置的作用很多,可以用来混合气体,也可以与圆底烧杯相接导管的气泡速度与直玻管中气泡速度之比为2:1(SO2与O2的气泡之比为2:1);干燥气体。
点评:本题考查了三氧化硫的制备实验,解答该题的关键是要分析该题的各个小装置作用,本题有利于培养学生分析实验的能力,该题难度适中。
本题难度:一般
3、选择题 常温下,向20L的真空容器中通入amolH2S和bmolCl2(a、b均为正整数,且a≤5,b≤5)。反应完成后,容器内气体可能达到的最大密度是……( )
A.17.85g/L
B.18.00g/L
C.18.25g/L
D.18.50g/L
参考答案:C
本题解析:由反应H2S+Cl2=2HCl+S可知H2S和Cl2物质的量均为5mol,容器内生成10molHCl,密度最大为:(36.5g/mol×10mol)/20L=18.25g/L。
该题容易错选A,认为H2S为1mol、Cl2为5mol,反应后剩余Cl2而密度最大,与SO2、H2S的混合混淆,H2S与SO2反应后生成固体S和液态水,但H2S与Cl2反应后有气体HCl生成,反应特点不同,应注意区分
本题难度:一般
4、计算题 某化学小组为了测定石膏(CaSO4・xH2O)的组成,即测定x值,做如下实验:将石膏加热使之脱水,加热过程中固体的质量与时间的变化关系如下图所示。数据表明当固体的质量为2.72g后不再改变。
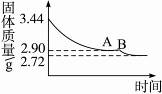
求(必须写出计算过程):
(1)石膏的化学式。
(2)图象中AB段对应化合物的化学式。
参考答案:(1)CaSO4・2H2O?(2)2CaSO4・H2O或CaSO4・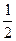 H2O
H2O
本题解析:(1)CaSO4・xH2O CaSO4+xH2O
CaSO4+xH2O
136+18x?136?18x
3.44g?2.72g0.72g
x=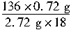 =2
=2
该化合物化学式为CaSO4・2H2O。
(2)实验数据和图象AB段说明在石膏受热分解过程中,有一固定组成的化合物存在。
CaSO4・2H2O  ?CaSO4・yH2O+(2-y)H2O
?CaSO4・yH2O+(2-y)H2O
172? 136+18y
3.44g? 2.90g
解得y=0.5
该化合物化学式为2CaCO4・H2O(或CaSO4・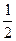 H2O)。
H2O)。
本题难度:简单
5、计算题 (8分)为测定钢铁中硫的含量,称取0.500g试样,高温下在氧气流中燃烧,使试样中的硫全部转化为二氧化硫。将燃烧后的气体通入加有淀粉指示剂的溶液中吸收,并用已知浓度的碘溶液进行滴定。
(1)滴定过程中反应的化学方程式是__________________________。
(2)若到达滴定终点时,消耗VmL浓度为amol・L-1的碘溶液,则试 样中硫的质量分数的计算式(请化简)为_____________________________。
样中硫的质量分数的计算式(请化简)为_____________________________。
(3)为了快速测定结果,配制一定浓度的碘溶液时,要使每消耗0.1mL碘溶液相当于试样中含硫0.001%。则该碘溶液的物质的量浓度应是多少?(需列简要计算过程)
参考答案:(8分)
(1)I2+SO2+2H2O ==H2SO4+2HI?(2分)
(2)6.4aV%?(2分)
(3)1.56×10-3mol・L-1?(4分)
本题解析:略
本题难度:一般