1������� ��12�֣�������Ҫ��ϡ��Ԫ�أ�Ӧ�÷dz��㷺����Ӧ����ѹ����ϡ�����������
��֪�������ǽϻ��ý������ڿ������ױ�������������������������ˮ�����
��
����
| �۵㣨�棩
| �е㣨�棩
|
��
| 841
| 1487
|
��
| 920
| 3470
|
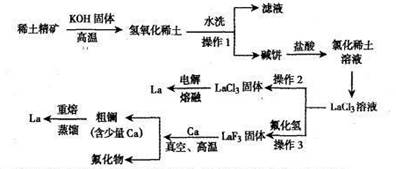
��1������1��3����ͬ��������������?��
��2������2��Ҫ��HCl����ķ�Χ�ڼ��ȵ�ԭ����?��
��3����������β��Ҫ�ü�Һ���գ���д����Ӧ�����ӷ���ʽ??��
��4����ա����¹����еķ�Ӧ����ʽΪ?��

��5�����羫�ƹ������¶ȿ��Ʒ�Χ?��
��6�����������Ƶõ�������Ȼ���м������ĸơ�ij���β�Ʒ69.709g������������0.209g���ò�Ʒ�ĵȼ�Ϊ?��������Ʒ�ȼ������ż�����99.8������������99.7������ѧ����99.5����.
�ο��𰸣���1�����ˣ���2����ֹLaCl3ˮ�⣻��3��Cl2+2OH-=Cl-+ClO-+H2O��
��4��3Ca+2LaF3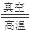 3CaF2+2La����5��1487��3470��C����6��������
3CaF2+2La����5��1487��3470��C����6��������
�����������1������1��3����ͬ���������Ƿ��������Թ�����Һ������ķ������������ǹ��ˡ���2����LaCl3��Һ�л��LaCl3���壬���ڸ�����ǿ�������Σ�������ˮ�ⷴӦ������Ϊ�˷�ֹ��ˮ�⣬����2Ҫ��HCl����ķ�Χ�ڼ��ȡ���3��2LaCl3 2La+ 3Cl2��.��β���к���������Ҫ�ü�Һ���գ��÷�Ӧ�����ӷ���ʽ��Cl2+2OH-=Cl-+ClO-+H2O����4����������ͼ��֪������ա����¹����еķ�Ӧ����ʽΪ3Ca+2LaF3
2La+ 3Cl2��.��β���к���������Ҫ�ü�Һ���գ��÷�Ӧ�����ӷ���ʽ��Cl2+2OH-=Cl-+ClO-+H2O����4����������ͼ��֪������ա����¹����еķ�Ӧ����ʽΪ3Ca+2LaF3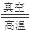 3CaF2+2La����5���ڴ����к�������Ca������Ca�ķе���1487�棬La�ķе���3470�棬���Ծ��ƹ������¶ȿ��Ʒ�Χ1487��3470�棻��6���ڸò�Ʒ��La������������{(69.709g-0.209g)��69.709g}��100%=99.7�����������ڷ�������
3CaF2+2La����5���ڴ����к�������Ca������Ca�ķе���1487�棬La�ķе���3470�棬���Ծ��ƹ������¶ȿ��Ʒ�Χ1487��3470�棻��6���ڸò�Ʒ��La������������{(69.709g-0.209g)��69.709g}��100%=99.7�����������ڷ�������
�����Ѷȣ�һ��
2��ѡ���� ��ͬ�¶��µ����ʵ���Ũ�ȵ�������Һ�У�pHֵ��С����
A��
B��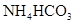
C��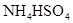
D��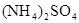
�ο��𰸣�C
���������NH4Cl��(NH4)2SO4�Աȣ�ˮ�ⶼ�����ԣ�(NH4)2SO4pH��С��NH4HCO3ˮ��ʼ��ԣ�pH���NH4HSO4Ϊ��ʽ�Σ�HSO4-��ȫ���룬��Һ������ǿ����pH��С��
�����Ѷȣ�һ��
3��ѡ���� ��0.1mol������������1Lˮ�У���ֽ������Һ���������������ǡ�������������
A��KCl
B��Mg(OH)2
C��Na2CO3
D��MgSO4
�ο��𰸣�C
�����������ΪMg(OH)2���ܣ��ʵ������OH�����٣������ų�Bѡ�A��C��D�����е���������ˮ�����������Ŀ�������ӣ�����A��D���е�Cl����SO42������ǿ��������������ˮ�⣬����Һ�в��ܲ����������ӣ������ǵ�ͬ�ģ�Cѡ���е�����������Һ�в���ˮ�⣻CO32��+H2O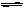 HCO3��+OH���������������Һ�е���������Ŀ��
HCO3��+OH���������������Һ�е���������Ŀ��
�����Ѷȣ�һ��
4��ѡ���� ����˵������ȷ����
A�����Ȼ�ϡ��NH4Cl��Һ��NH4Cl ˮ��̶Ⱦ�����
B�����з�̪��Һ�İ�ˮ�м���NH4Cl���壬��Һ��ɫ��dz
C������NH4Cl�İ�ˮ�У�[NH4+]���ܴ���[Cl-]
D����ˮ�м�������NH4Cl���壬�ָ���ԭ�¶ȣ�ˮ�ĵ���ƽ�������ҵ��볣�����
�ο��𰸣�D
���������A�������ˮ��Ϊ���ȷ�Ӧ������NH4Clˮ��̶�����ϡ��NH4Cl��Һ��ˮ��̶�������ȷ��B�����з�̪��Һ�İ�ˮ�м���NH4Cl���壬������NH4+Ũ�ȣ�ʹ��ˮ�ĵ���̶ȼ�С����Һ��ɫ��dz����ȷ��C������ˮ�����϶࣬��ˮ�����NH4+��[NH4+]����[Cl-]����ȷ��D������NH4Cl��NH4+����ˮ�ⷴӦ���ָ���ԭ�¶ȣ�ˮ�ĵ���ƽ�����Ƶ����볣�����䣬����
�����Ѷȣ�һ��
5��ѡ���� �����й����ʵ���Ũ�ȹ�ϵ��ȷ����?
A�����ʵ���Ũ�����CH3COOH��CH3COONa��Һ�������ϣ���Һ�����ԣ�
c(CH3COO��)��c(CH3COOH)
B��pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��
c(NaOH)��c(CH3COONa)��c(Na2CO3)
C��0.1 mol��L��1��NaHA��Һ����pH��4��c(HA��)��c(H+)��c(H2A)��c(A2��)
D��pH��2��HA��Һ��pH��12��MOH��Һ����Ȼ�Ϻ���Һ������Ũ�ȹ�ϵ��
c(H+)��c(M+)��c(OH��)��c(A��)?
�ο��𰸣�D
���������A����Һ�������ԣ�����B��pH���ʱ��c(NaOH)��c(Na2CO3)��c(CH3COONa)������C��c(HA��)��c(H+)��c(A2��)��c(H2A)������D������������������غ㡣
�����Ѷȣ�һ��