1、选择题 充分利用能源、提高原子利用率、减少向环境排放废弃物等都是“绿色化学”的基本要求。 ?①?实验室短时间保存硫酸亚铁溶液时,向试剂瓶中添加铁钉和少量稀硫酸;?②?用稀硝酸代替浓硝酸溶解、回收做银镜实验后试管内壁的银;?③接触法制硫酸的设备中安装“热交换器”和锅炉,利用余热预热冷原料气和蒸气发电;?④工业合成氨中分离产物得到氢气和氮气再循环使用。上述主要不是从“绿色化学”角度考虑的是
[? ]
A.只有①?
B.②④?
C.③④?
D.②③
参考答案:A
本题解析:
本题难度:简单
2、选择题 合成氨工业上采用循环操作的原因主要是(? )
A.加快反应速率
B.能提高NH3的平衡浓度
C.降低NH3的沸点
D.提高N2和H2的利用率
参考答案:D
本题解析:合成氨工业上采用循环操作的原因主要是提高原料的利用率即提高N2和H2的利用率,提高经济效益。
本题难度:简单
3、选择题 关于工业生产的下列叙述中,不正确的是
A.工业生产硫酸时,使用热交换器可以充分利用反应中所放出的热量
B.工业上合成氨没有采用更大的压强是从设备和动力要求方面考虑的
C.工业上用离子交换膜法电解饱和食盐水制烧碱
D.工业上采用电解熔融氯化铝的方法制取金属铝
参考答案:D
本题解析:略
本题难度:简单
4、填空题 马格尼特法冶炼镁的工艺流程如下图。炉料中除有煅烧白云石和硅铁外,还加入煅烧过的铝土矿,加Al2O3的主要目的是降低渣的熔点,便于液态排渣。
已知白云石的成分为CaCO3・MgCO3,硅铁是指含有55%硅左右的铁[可表示为Si(Fe)],作还原剂,最后得到低品位的硅铁[可表示为Fe(Si)],简易流程图如下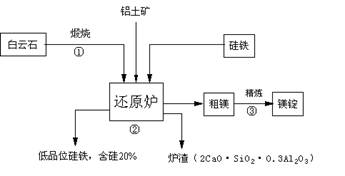
试回答下列问题
(1)反应①,白云石煅烧得CaO・MgO的化学方程式为:?。
(2)反应②,还原炉中发生反应生成镁和炉渣的化学方程式为:?。
(3)该成分的沪渣是一种工业生产的重要原料,可作为生产?原料。
(4)马格尼特法冶炼镁,一台4500千瓦的炉子可日产约7.2吨镁,一天至少约消耗含硅60%的硅铁?吨。
参考答案:
(1)CaCO3・MgCO3 CaO・MgO+2CO2↑
CaO・MgO+2CO2↑
(2)2(CaO・MgO)+Si(Fe)+0.3Al2O3? ?2Mg+2CaO・SiO2・0.3Al2O3+Fe(Si)
?2Mg+2CaO・SiO2・0.3Al2O3+Fe(Si)
[或:2(CaO・MgO)+Si+0.3Al2O3? ?2Mg+2CaO・SiO2・0.3Al2O3]
?2Mg+2CaO・SiO2・0.3Al2O3]
(3)水泥?(4)8.4t
本题解析:
本题考查工艺流程中镁的冶炼。(2)由题中所述和流程中的信息,还原炉中为白云石煅烧产物与硅铁、铝土矿发生氧化还原反应,生成炉渣、镁以及低品位的硅铁,方程式为:2(CaO・MgO)+Si(Fe)+0.3Al2O3? ?2Mg+2CaO・SiO2・0.3Al2O3+Fe(Si);(3)该炉渣主要成分为硅酸盐,可以用来生成水泥等硅酸盐产品;(4)由关系:
?2Mg+2CaO・SiO2・0.3Al2O3+Fe(Si);(3)该炉渣主要成分为硅酸盐,可以用来生成水泥等硅酸盐产品;(4)由关系:
2Mg~Si
48? 28
7.2? x
X=4.2t
进矿渣的硅为4.2t。
设原有硅0.6x,进入低品硅铁中有硅0.6x-4.2
反应后,低品位硅铁变成了:x-4.2,可得: =0.2,x=8.4t。
本题难度:一般
5、选择题 化学工业在经济发展中的作用举足轻重。下列有关工业生产的叙述中,正确的是? (? )
A.硫酸生产中常采用高压条件来提高SO2的转化率
B.合成氨中采用及时分离液态氨来提高反应速率
C.电解精炼铜中,溶液中c(Cu2+)基本保持不变
D.氯碱工业中阳极得到氢氧化钠和氢气
参考答案:C
本题解析:2SO2+O2 2SO3,该反应在常压下转化率非常高,不需要采用高压来提高转化率;N2+3H2
2SO3,该反应在常压下转化率非常高,不需要采用高压来提高转化率;N2+3H2 2NH3,由于NH3液化后使混合气体中c(NH3)降低,引起v(正),v(逆)均降低;电解精炼铜时,阳极反应式为Cu-2e-=Cu2+,阴极反应式为Cu2++2e-=Cu,所以溶液中c(Cu2+)基本保持不变;
2NH3,由于NH3液化后使混合气体中c(NH3)降低,引起v(正),v(逆)均降低;电解精炼铜时,阳极反应式为Cu-2e-=Cu2+,阴极反应式为Cu2++2e-=Cu,所以溶液中c(Cu2+)基本保持不变;
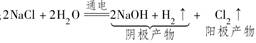 ?D错误。
?D错误。
本题难度:一般