1、填空题 (14分)已知25℃、101kPa下,氢气、甲烷和葡萄糖的燃烧热依次为285.8 kJ/mol、890.3kJ/mol、2800 kJ/mol。
(1)0.1mol甲烷和0.2mol氢气组成的混合气体在25℃、101kPa下完全燃烧释放的热量为 ;
(2)写出表示葡萄糖燃烧热的热化学方程式: ;
(3)有人利用甲烷和氧气的反应设计成如图所示燃料电池,若使用酸性电解质溶液,则两极的电极反应式为:
a极: ,b极: ;
若使用碱性电解质溶液,则b极的电极反应式为:b极: ;
放电时电极a作 极,外电路中电流从 流向 ,电解质溶液中阳离子移向 极;
参考答案:(14分)(1) (2分/个) 146.19kJ/mol
(2) C6H12O6(s) + 6O2(g) 6CO2(g) + 6H2O(l) △H= -2800kJ/mol
6CO2(g) + 6H2O(l) △H= -2800kJ/mol
(3)a极:2O2+ 8H++ 8e-=== 4H2O ;b极:CH4+ 2H2O -8e-===CO2+ 8H+
b极:CH4+ 10OH--8e-===CO32-+7H2O
(1分/个) 正 a b a
本题解析:略
本题难度:简单
2、选择题 向pH=1的某酸溶液和pH=13的氢氧化钠溶液中,加入足量的铝片,放出H2的物质的量之比为3:1其原因可能是
A.两溶液的体积相同,酸是多元强酸
B.若酸为一元强酸,酸溶液的体积是碱溶液体积的3倍
C.两溶液的体积相同,酸是弱酸
D.酸是强酸,且酸溶液的浓度比NaOH溶液浓度大
参考答案:C
本题解析:略
本题难度:一般
3、填空题 已知1molCO气体完全燃烧生成CO2气体放出283kJ的热量,1molH2气体完全燃烧生成液态水放出286kJ的热量,1molCH4气体完全燃烧生成CO2气体和液态水放出890kJ的热量
(1)写出H2完全燃烧的热化学方程式____________ 。
(2)若1molCH4气体完全燃烧生成CO2气体和水蒸气放出的热量__________ 890kJ (填>、<或=)(3)若将amolCH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,放出热量(Q)的取值范围是_____________ 。
(4)若将amolCH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,且CO2和水的物质的量相等时,放出热量(Q)的取值范围是____________ 。
参考答案:(1)H2(g)+1/2O2(g)==H2O(l);△H = - 286kJ /mo1
(2)<
(3)283akJ<Q<890akJ
(4)284.5akJ<Q<586.5akJ
本题解析:
本题难度:困难
4、选择题 下列说法中不正确的是
A.与煤油、柴油相比较,天然气是一种比较清洁的化石燃料
B.乙醇是一种可再生能源,作为燃料的优点的是完全燃烧的产物不污染环境
C.利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量
D.煤的气化和液化不仅可以获得洁净燃料,而且再燃烧会放出更多的热量
参考答案:D
本题解析:天然气的主要成分是甲烷,完全燃烧的生成物是CO2和水,属于清洁燃料,选项A正确;乙醇属于可再生能源,其燃烧产物是水和CO2,不会造成环境污染,选项B正确;太阳能、风能和氢能等均是新能源,不会造成环境污染,替代化石能源能有效改善空气质量,选项C正确;根据能量守恒定律可知,煤的气化和液化可以获得洁净燃料,但再燃烧不会放出更多的热量,选项D不正确,答案选D。
点评:化学与可持续发展及环境保护尽管不是教学的重点,但该内容与我们的生产、生活息息相关,因此成为历年高考的必考的热点。试题的命题形式是常把化学知识与实际生产、生活、环境保护及科技前沿等问题结合起来,突出化学与可持续发展、环境保护的密切联系,综合考查学生分析问题、解决问题的能力,可很好的落实新课标的理念。
本题难度:一般
5、计算题 硫酸和盐酸的混合溶液20mL,在这溶液中加入0.025 mol/L氢氧化钡溶液时生成硫酸钡的量和溶液的pH值如图所示。
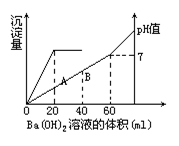
试计算:
(1)最初溶液中硫酸和盐酸的物质的量浓度
(2)A、B两点溶液的 pH值(溶液混合时体积变化忽略不计,pH值可以保留对数形式)。
参考答案:(1)[H2SO4]="0.025" mol/L,[HCl]= 0.10 mol/L
(2)pHA="2-1g5" pHB=2-1g1.67
本题解析:如图中曲线表明:跟硫酸反应生成硫酸钡沉淀消耗Ba(OH)2溶液20mL;而跟硫酸,盐酸进行中和反应,消耗Ba(OH)2溶液60mL。
(1)H2SO4+Ba(OH2)=BaSO4↓+2H2O?①
2HCl+Ba(OH)2=BaCl2+2H2O?②
反应①中,消耗Ba(OH)2的物质的量=0.025×0.020=5.0×10-4mol,

="0.10" mol/L。
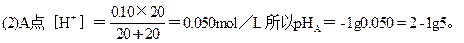
B点H2SO4已被中和完全,部分HCl被中和。
已被中和的HCl的物质的量=0.025×(40-20)×10-3×2=1.0×10-3mol
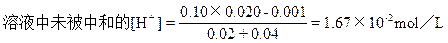
所以,pHB=-1g1.67×10-2=2-1g1.67。
本题难度:一般