1、选择题 关于化学平衡常数的叙述中,正确的是(?)
A.只与化学方程式本身和温度有关
B.只与反应温度有关
C.与化学方程式本身和温度有关,并且会受到起始浓度的影响
D.只与化学方程式本身有关,与其它任何条件无关的一个不变的常数
参考答案:A
本题解析:大量事实证明,化学平衡常数决定于两个方面的因素:化学方程式本身和反应体系的温度,与起始浓度等其它任何外界条件无关。
本题难度:一般
2、选择题 在相同条件下(T=500k),相同体积甲、乙两容器,甲充入1g SO2、1g O2,乙充入2g SO2、2g O2.下列叙述错误的是
A.化学反应速率乙>甲
B.平衡后O2浓度乙>甲
C.SO2转化率乙>甲
D.平衡后SO2的体积分数乙>甲
参考答案:D
本题解析:A正确,化学反应速率与浓度大小有关,相同条件下,反应物的浓度越大,反应速率越快;B正确,由于乙的投量更多,即平衡后O2浓度乙>甲;C正确,乙的反应相当于两个甲叠加,即相当于增大压强,平衡向气体体积减少的方向移动,所以SO2转化率乙>甲;D错,由于乙的反应物转化率更高,所以平衡后SO2的体积分数甲>乙;
本题难度:困难
3、选择题 对于可逆反应2NO2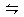 N2O4,下列说法能证明反应已达平衡状态的是?
N2O4,下列说法能证明反应已达平衡状态的是?
⑴温度和体积一定时,某一生成物浓度不再变化;
⑵温度和体积一定时,容器内压强不再变化;
⑶条件一定,混合气体的平均相对分子质量不再变化;
⑷温度和体积一定时,混合气体的颜色不再发生变化;
⑸温度和压强一定时,混合气体的密度不再发生变化;
参考答案:⑴⑵⑶⑷⑸
本题解析:⑴条件一定时,某一生成物浓度不再变化,说明了“定”的真正含义,故正确;⑵此反应前后气体体积不相等,当温度、体积一定时,压强不变能说明任何物质的物质的量不变,为“定”值,故反应已达平衡状态;⑶此反应前后气体物质的量不相等,质量不变,混合气体的平均相对分子质量不再变化能说明任何物质的物质的量不变,为“定”值,故反应已达平衡;⑷混合气体的颜色不再发生变化,说明各物质的浓度不变,证明反应已达平衡状态;⑸此反应前后气体物质的量不相等,当温度、压强一定时,体积不变,密度不变,能说明反应已达平衡状态。
本题难度:一般
4、选择题 可逆反应
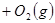

 从正方向开始,并达到了平衡,此时
从正方向开始,并达到了平衡,此时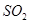 和
和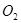 的物质的量之比为2:1,若采取某种措施,导致
的物质的量之比为2:1,若采取某种措施,导致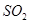 和
和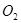 又消耗了一些,并再次达到平衡,下列说法正确的是
又消耗了一些,并再次达到平衡,下列说法正确的是
A.新平衡体系中,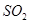 和
和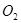 物质的量之比仍为2:1
物质的量之比仍为2:1
B.平衡向正反应方向移动,原因是正反应速率增大,逆反应速率减小
C.新平衡体系与旧平衡体系比较,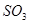 的浓度肯定增大
的浓度肯定增大
D.若所采取的措施是缩小容器的容积,则新旧平衡中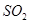 和
和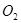 的转化率之比都是1:1
的转化率之比都是1:1
参考答案:D
本题解析:A.若通过增大反应物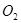 的浓度导致
的浓度导致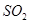 和
和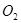 又消耗了一些,则新平衡体系中
又消耗了一些,则新平衡体系中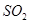 和
和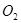 物质的量之比就不是2:1。B. 平衡向正反应方向移动,是因为正反应速率大于逆反应速率。C.如果通过减小
物质的量之比就不是2:1。B. 平衡向正反应方向移动,是因为正反应速率大于逆反应速率。C.如果通过减小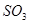 的浓度导致
的浓度导致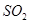 和
和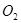 又消耗了一些,则新平衡时
又消耗了一些,则新平衡时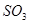 的浓度比原平衡小
的浓度比原平衡小
本题难度:一般
5、选择题 下列事实不能用勒夏特列原理解释的是
①由H2、I2蒸气、HI气体组成的平衡体系加压后颜色变深
②黄绿色的氯水光照后颜色变浅
③使用催化剂可加快SO2转化为SO3的速率
④在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
A.②③
B.②④
C.①③
D.①④
参考答案:C
本题解析:如果改变影响平衡的1个条件,则平衡就向能够减弱这种改变的方向移动,这就是勒夏特列原理。应用氢气和碘反应生成碘化氢的反应是体积不变的可逆反应,所以改变压强平衡不移动,颜色变深是因为碘的浓度变大导致的,①不能。催化剂只能影响反应速率,但不能改变平衡状态,所以不能用勒夏特列原理解释,其余都是正确的,答案选C。
本题难度:一般