1、选择题 下列各组离子,在水溶液中能大量共存的是
A.K+、H+、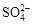 、OH-
、OH-
B.Na+、H+、Cl-、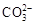
C.Na+、Ca2+、 、
、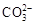
D.Na+、Cu2+、Cl-、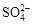
参考答案:D
本题解析:A项中H+和OH-不能大量共存;B项中H+和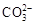 不能大量共存;C项中Ca2+和
不能大量共存;C项中Ca2+和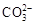 不能大量共存。答案选D。
不能大量共存。答案选D。
点评:离子不能大量共存的一般情况是:(1)能发生复分解反应的离子之间(即生成沉淀,气体,水、弱酸、弱碱等难电离物质);(2)能生成难溶物的离子之间(如:Ca2+和 SO42-;Ag+和 SO42-);(3)能完全水解的离子之间,如多元弱酸和弱碱盐的阴、阳离子(如:Al3+, Fe3+与 CO32-、HCO3-、AlO2-、ClO-,S2-等);(4)能发生氧化还原反应的离子之间(如:Fe 、H+、NO3-;S2-、ClO-;S2-、 Fe3+等);(5)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。
本题难度:简单
2、选择题 在下列溶液中,各组离子一定能够大量共存的是
[? ]
A.使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+
B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
C.c(H+) =10-12mol/L的溶液:K+、Ba2+、Cl-、Br-
D.碳酸氢钠溶液:K+、SO42-、Cl-、H+
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列有关镁及其化合物的离子方程式书写正确的是
A.MgCO3与盐酸反应:CO32-+2H+ ="=" CO2↑+H2O
B.Mg(OH)2与H2SO4反应:Mg2++2OH-+2H++SO42- ="=" MgSO4↓+2H2O
C.镁与醋酸反应:Mg+2H+ ="=" Mg2++H2↑
D.工业上以海水为原料制备Mg(OH)2:Ca(OH)2+Mg2+ ="=" Mg(OH)2↓+Ca2+
参考答案:D
本题解析:碳酸镁不溶于水,应该用化学式表示,A不正确;氢氧化镁也是不溶于水的,应该用化学式表示;醋酸是难电离的,应该用化学式表示,所以正确的答案选D。
点评:用实际参加反应的离子表示的方程式是离子方程式。书写离子方程式的关键是准确判断出哪些物质用化学式表示,哪些物质用离子符号表示。只有同时满足易溶、易电离的物质才能用离子表示,其余全部是用化学式表示,据此可以进行有关的书写和判断。
本题难度:一般
4、选择题 在强碱性溶液中能大量共存,并且溶液为无色透明的离子组是(?)
A.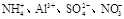
B.K+、Na+、[Al(OH)4]-、NO3-
C.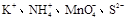
D.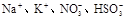
参考答案:B
本题解析:离子间如果发生化学反应,则不能大量共存,反之不能大量共存。溶液显强碱性,所以NH4+和HSO3-都不能大量共存,答案选B。
本题难度:一般
5、选择题 下列各组离子在溶液中按括号内的物质的量之比混合,得到无色、碱性、澄清溶液的是( )
A.Na+、Al3+、Cl-、OH-(5:1:4:4)
B.NH4+、Ba2+、OH-、Cl-(1:1:1:2)
C.Fe3+、Na+、Cl-、S2-(1:2:3:1)
D.K+、H+、I-、HCO3-(1:1:1:1)
参考答案:A.Al3+、OH-以1:4反应生成偏铝酸钠,得到无色、碱性、澄清溶液,故A正确;
B.NH4+、OH-以1:1反应生成一水合氨,得到无色、碱性、澄清溶液,故B正确;
C.Fe3+、S2-发生氧化还原反应生成亚铁离子和S,得到浅绿色溶液,故C错误;
D.H+、HCO3-结合生成水和气体,溶液为弱酸性,不是碱性溶液,故D错误;
故选AB.
本题解析:
本题难度:简单