1、简答题 (14分)甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。

(1)B中反应的离子方程式是____。
(2)A中溶液变红的原因是____。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在?。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是SCN―与Cl2发生了反应。
(4)甲同学猜想SCN―可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN―的电子式为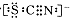
①甲同学认为SCN―中碳元素没有被氧化,理由是?。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN―中被氧化的元素是?。
③通过实验证明了SCN―中氮元素转化为NO3-,他的实验方案是____。
④若SCN―与Cl2反应生成1 mol CO2,则转移电子的物质的量是?mol。
参考答案:(14分)
(1)Cl2+2 OH-= Cl-+ ClO-+ H2O;
(2)Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色Fe(SCN)3,所以溶液变红
(3)①Fe3+
(4)①SCN-中的碳元素是最高价态+4价
②硫元素
③取足量铜粉于试管中,加入A中黄色溶液和一定量的盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在NO3-,SCN-中氮元素被氧化成NO3-;
④16
本题解析:(1)B中是氯气与氢氧化钠的反应,离子方程式为Cl2+2 OH-= Cl-+ ClO-+ H2O;
(2)A中的Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色Fe(SCN)3,所以溶液变红
(3)①加入NaOH溶液,有红褐色沉淀生成,此红褐色沉淀为氢氧化铁沉淀,则溶液中一定存在Fe3+
(4)①因为SCN―中碳元素已经是最高价态+4价;
②与盐酸酸化的BaCl2溶液,产生白色沉淀,此白色沉淀为硫酸钡沉淀,所以被氧化的元素是硫元素;
③证明SCN―中氮元素转化为NO3-,利用硝酸的强氧化性,被还原的产物是红棕色气体,可证明SCN―中氮元素转化为NO3-,
④SCN―与Cl2反应生成1 mol CO2,说明有1mol的SCN―与Cl2反应,SCN―中的-2价S、-3价N化合价升高到+6价、+5价,失电子总数为8+8=16mol,所以转移电子的物质的量为16mol。2与FeCl2和KSCN混合溶液的反应实验,离子检验,根据元素价态判断发生的反应,电子转移数目的确定
本题难度:一般
2、选择题 下列反应不能生成FeCl2的是
A.铁和CuCl2溶液反应
B.FeCl3溶液中加入铜粉
C.铁在氯气中燃烧
D.铁和稀盐酸反应
参考答案:C
本题解析:A中铁置换铜,产生氯化亚铁,B中反应产生氯化铜和氯化亚铁,C中生成的是三氯化铁而不是氯化亚铁,D中反应生成氯化亚铁和氢气。
点评:由于氯气氧化性强,所以直接把铁氧化为三价铁。
本题难度:一般
3、实验题 (16分)钢铁工业是国家工业的基础,是日常生活中用途最广、用量最大的金属材料。
(1)常温下,可用铁质容器盛装浓硫酸的原因是?。
(2)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6mol/L盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。
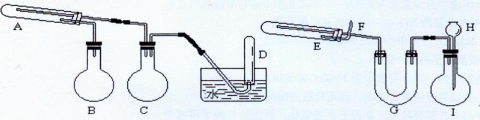
填写下列空白:
①实验进行时试管A中应加入的试剂是?;烧瓶B的作用是?;烧瓶C的作用是?。
②实验时,U型管G中加入的试剂是?;长颈漏斗H中应加入?。
③试管E中发生反应的化学方程式是?。
④为了安全,在E管中的反应发生前,在F出口处必须?。
参考答案:

本题解析:
(1)常温下,铁在浓硫酸中发生钝化现象使铁表面形成一层致密稳定的氧化膜,故铁制品容器可以盛放浓硫酸,故答案为:浓硫酸使铁表面形成一层致密稳定的氧化膜;
⑵①根据题干中所提供的物质可以推断出第一步实验中除了生成四氧化三铁外还会生成氢气,发生的反应为铁在高温和水蒸气反应生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O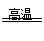 4H2+Fe3O4;试管A是铁与水蒸气反应的装置,故在A中装的应该是普通铁粉,在反应过程中 要生成氢气,所以D是用来收集氢气的,烧瓶的作用就是加热液体或者对液体进行蒸馏,所以这里蒸馏瓶所起的作用就是产生水蒸气,为了防止向试管中通入水蒸气使试管骤冷,引起水的倒流从而在试管和收集气体的试管中间加上了广口瓶,保证实验安全;A中是铁和水蒸气的反应;B中为产生水蒸气的装置,C为安全瓶防止倒吸的作用,D中收集的是氢气,
4H2+Fe3O4;试管A是铁与水蒸气反应的装置,故在A中装的应该是普通铁粉,在反应过程中 要生成氢气,所以D是用来收集氢气的,烧瓶的作用就是加热液体或者对液体进行蒸馏,所以这里蒸馏瓶所起的作用就是产生水蒸气,为了防止向试管中通入水蒸气使试管骤冷,引起水的倒流从而在试管和收集气体的试管中间加上了广口瓶,保证实验安全;A中是铁和水蒸气的反应;B中为产生水蒸气的装置,C为安全瓶防止倒吸的作用,D中收集的是氢气,
故答案为:普通铁粉(或铁粉);产生水蒸气;防止水倒吸(或用作安全瓶);氢气;
②装置I是用来制取氢气的装置,所以装置H是用来添加盐酸的,F中发生反应:Fe3O4+4H2 3Fe+4H2O;由于使用的是稀盐酸来制取氢气,所以在产生氢气的同时可能带出部分水蒸气和氯化氢气体,故在U型管中加入固体来干燥气体,吸收氯化氢和水蒸气,所以U型管中为固体NaOH(或碱石灰、CaO等碱性固体干燥剂),
3Fe+4H2O;由于使用的是稀盐酸来制取氢气,所以在产生氢气的同时可能带出部分水蒸气和氯化氢气体,故在U型管中加入固体来干燥气体,吸收氯化氢和水蒸气,所以U型管中为固体NaOH(或碱石灰、CaO等碱性固体干燥剂),
故答案为:固体NaOH(或碱石灰、CaO等碱性固体干燥剂);6摩/升的稀盐酸;
③依据装置和实验目的分析,试管E中发生反应是氢气还原四氧化三铁的反应,反应的化学方程式是:Fe3O4+4H2 3Fe+4H2O,故答案为:Fe3O4+4H2
3Fe+4H2O,故答案为:Fe3O4+4H2 3Fe+4H2O;
3Fe+4H2O;
④氢气是可燃性气体,做氢气的性质实验时必须保证氢气是纯净的,为了安全,在E管中的反应发生前,在F出口处必须进行气体验证纯度;E管中的反应开始后,在F出口处应点燃氢气,避免排放到空气中遇火爆炸;故答案为:检验氢气的纯度;点燃氢气.
本题难度:一般
4、计算题 (6分)将足量铁投入到200mLH2SO4和CuSO4的混和溶液中,充分反应后,产生H21.12L(标准状况),铁块的质量减轻了1.2g。求原溶液中c(H2SO4)及c(CuSO4)。(假设反应前后溶液的体积不变)
参考答案:
Fe?+? H2SO4?=? FeSO4?+? H2↑
56g? 1mol? 22.4L
m1(Fe)? n(H2SO4)? 1.12L
m1(Fe)=
n(H2SO4)=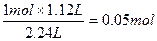
V(液)=V(H2SO4)=V(CuSO4)=200mL=0.2L
C(H2SO4)=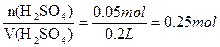
Fe?+? CuSO4? ?=? FeSO4?+? Cu
?=? FeSO4?+? Cu
56g? 1mol? 64g
m2(Fe)? n(CuSO4)? m(Cu)
m(Cu)=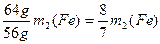
由题意得:m1(Fe) +m2(Fe)-m(Cu)=1.2g
2.8g+m2(Fe)-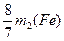 =1.2g
=1.2g
m2(Fe)=11.2g
n(CuSO4)=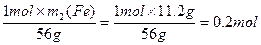
c(CuSO4)=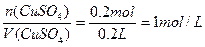
本题解析:略
本题难度:一般
5、选择题 有一种物质俗称铁红,常用作红色油漆和涂料,它的化学式为(? )
A.FeO
B.Fe2O3
C.Fe
D.Fe3O4
参考答案:B
本题解析:
铁在吸氧腐蚀时产生铁锈,此为原电池原理,负极2Fe-4e-=2Fe2+,正极4e-+O2+2H2O=4OH-,总反应式2Fe+O2+2H2O=2Fe(OH)2,氢氧化亚铁被空气中的氧气氧化为氢氧化铁,氢氧化铁再分解生成氧化铁Fe2O3,这是红色物质,俗称铁红。
本题难度:简单