1、选择题 某溶液中有Mg2+、Fe2+、Fe3+和Al3+四种阳离子,若向其中加入过量的NaOH溶液,微热并搅拌,过滤,在滤渣中再加入过量的盐酸,所得溶液中含有的阳离子是( )
A.Mg2+
B.Fe2+
C.Fe3+
D.Al3+
参考答案:AC
本题解析:
本题难度:一般
2、填空题 无水硝酸铜极易吸水,加热到210℃升华,它和Cu(NO3)2 ・3H2O晶体的化学性质有较大差异, Cu(NO3)2 ・3H2O晶体加热到170℃分解。已知:乙酸乙酯的沸点为77 ℃。
(1)加热蒸干Cu(NO3)2 溶液得不到无水硝酸铜的原因是_____________。
(2)将铜片加人到N2 O 4的乙酸乙酯溶液中可制得无水硝酸铜,同时生成NO,写出反应的化学方程式_____________;从乙酸乙醋中分离出无水硝酸铜的实验操作是_____________。
(3)为探究Cu(NO3)2 ・3H2O受热分解的产物,某探究小组利用下图装置进行实验。(图中夹持和加热装置去)
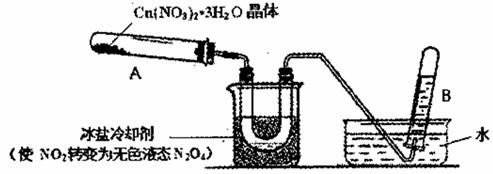
往试管A中加人研细的Cu(NO3)2 ・3H2O体并加热,观察到试管A中有红棕色气生成,最终残留黑色粉末;U型管中有液体生成,在试管B中收集到无色气体。
①当导管口不再有气池冒出时,反应停止,拆除装置的操作首先是______。
②试管B中收集到的气体一定含有______。
(4)锌与Cu(NO3)2溶液能发生反应。在一支试管中注人1 mol・L-1的Cu(NO3)2溶液,再放入一块锌片,观察到在反应初期有大量无色气泡冒出,同时锌片上析出红色固体。该小组猜想气体的成分,并设计的实验步骤,请填写下表。

参考答案:(1)Cu(NO3)2在溶液中易水解生成Cu(OH)2和易挥发的HNO3,加热,水解程度更大(2分)
(2)2N2O4+Cu=Cu(NO3)2+2NO↑(没配平扣1分,没“↑”不扣分,3分)蒸馏?(2分)
(3)①移出水槽中的导管B(其它合理答案也给分,2分)②O2(2分)(4)
设计的实验步骤
预期现象和结论
往小试管中注入空气(或使试管口露置于空气中)
若试管口气体变为红棕色,证明该气体是NO,反之不是。
将小试管的管口靠近火焰
若有爆鸣声,证明该气体是H2,反之不是
?
(上述实验两种方案,答对一种即给分,其它方案如合理也给分;结论为O2不给分,实验步骤1分,现象1分,结论2分,共4分)
本题解析:(1)Cu(NO3)2在溶液中易水解生成Cu(OH)2和易挥发的HNO3,水解吸热,加热,水解程度更大,因此加热蒸干Cu(NO3)2 溶液。
(2)将铜片加人到N2 O 4的乙酸乙酯溶液中可制得无水硝酸铜,同时生成NO,则根据原子守恒以及电荷守恒看写出该反应的化学方程式为2N2O4+Cu=Cu(NO3)2+2NO↑;由于乙酸乙酯的沸点为77 ℃,所以从乙酸乙醋中分离出无水硝酸铜的实验操作是蒸馏。
(3)①由于排水法收集气体时温度降低后容易倒吸,因此反应停止,拆除装置的操作首先是移出水槽中的导管B。
②试管A中有红棕色气生成,因此气体是NO2。最终残留黑色粉末,该黑色粉末应该是氧化铜;U型管中有液体生成,此时NO2转化为四氧化二氮。所以根据氧化还原反应中电子得失守恒可知,反应中一定还有氧化产物氧气产生,则在试管B中收集到无色气体一定含有氧气。
(4)硝酸铜溶液中铜离子水解溶液显酸性,另外NO3-还具有氧化性,因此锌与硝酸铜溶液反应生成的无色气体可能是氢气或NO。检验NO可以利用NO极易被氧化生成红棕色NO2来验证。而氢气是可燃性气体,所以可以利用爆鸣法进行验证。
本题难度:困难
3、填空题 (10分)已知X为Fe2O3和CuO的混合物,且知氧化性顺序:Fe3+>Cu2+>H+>Fe2+。取X样品进行如下图所示的实验:
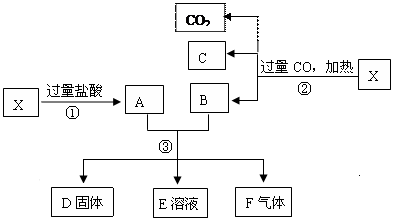
(1)写出③步可能发生反应的离子方程式为 ?。(共有3个)
(2)若溶液E中只有一种金属离子,则一定是?;若溶液E含有两种金属离子,则一定是?。
(3)若D固体是纯净物,该固体是?。(填化学式)
(4)印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路的离子反应方程式为?。
参考答案:(1)2Fe3+ + Fe ="3" Fe2+;Cu2++Fe=Fe2+ +Cu;2H++Fe=Fe2+ + H2 ↑?
(2)Fe2+;Fe2+、Cu2+?(3)Cu?(4)2Fe3+ + Cu =2Fe2+ + Cu2+
本题解析:略
本题难度:简单
4、选择题 常温下,不能用铁制容器存放的物质是
A.浓硫酸
B.浓硝酸
C.CuSO4溶液
D.稀氨水
参考答案:C
本题解析:浓硫酸、浓硝酸都可以使铁制容器发生钝化能用铁制容器存放,A、B不选;
CuSO4+Fe=" Fe" SO4+ Cu?,CuSO4溶液不能用铁制容器存放,稀氨水不与铁反应可用铁制容器存放。答案选C.
本题难度:简单
5、选择题 人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”;有一年很多地方的葡萄都减产甚至绝收,而法国小镇波尔多因为葡萄树都涂上了CuSO4与Ca(OH)2所以获得了大丰收。以下分析正确的是
A.CuSO4与Ca(OH)2含有葡萄生长所需的微量元素
B.CuSO4与Ca(OH)2混合物是化学肥料
C.Cu2+和碱可以使蛋白质变性,能杀死病菌,可以防治病虫害
D.CuSO4与Ca(OH)2混合物是有机农药,可以防治病虫害
参考答案:C
本题解析:强碱、重金属均可使蛋白质变性,能杀死病菌,可以防治病虫害,答案为C
本题难度:一般