1、填空题 如图甲、乙是电化学实验装置。
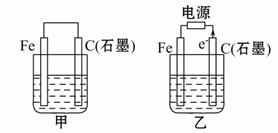
(1)若甲、乙两烧杯中均盛有饱和NaCl溶液。
①甲中石墨棒上的电极反应式为 ;
②乙中总反应的离子方程式为 ;
③将湿润的淀粉-KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为: ;
(2)若甲、乙两烧杯中均盛有CuSO4溶液。
①甲中铁棒上的电极反应式为: ;
②如果起始时乙中盛有200 mL pH = 5的CuSO4溶液(25 ℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入 (填写物质的化学式) g。
2、填空题 如图所示,若电解5 min时,铜电极质量增加2.16 g。
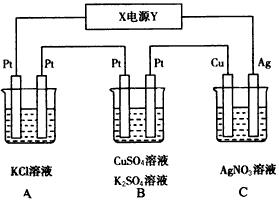
试回答:
(1)电源电极X名称为_______(填“正极”或“负极”)。
(2)电解池中溶液的pH变化:B_______,C_______(填“增大”“减小”或 “不变”)。
(3)B中的阳极的电极反应式为__________________;若通电5 min时B中共收集224 mL气体(标准状况)。
溶液体积为200 mL,则通电前硫酸铜溶液的物质的量浓度约为___________。
(4)A中发生反应的化学方程式为________________。若A中KCl溶液的体积也是200 mL,电解后溶液的pH=________。
(5)若将C装置单独取出,导线连接铜、银后,请写出负极的电极反应式________________
3、填空题 (8分)最近雾霾天气又开始肆虐我国大部分地区。其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该吸收反应的离子方程式是
(2)已知H2SO3的电离常数为 K1=1.54×10-2 , K2=1.02×10-7, H2CO3的电离常数为 K1=4.30×10-7, K2= 5.60×10-11, www.91eXam.org则下列微粒可以共存的是_____________。
A.CO32- HSO3- B.HCO3- HSO3-
C.SO32- HCO3- D.H2SO3 HCO3-
(3)吸收液吸收SO2的过程中,pH随n(SO3²
4、填空题 (4分)下图装置B中是浓度均为0.1mol/L的NaCl、CuSO 混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加____________g;此时,所有电极上总共收集到的气体的总体积为___________L(换算成标准状况下的体积)。
混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加____________g;此时,所有电极上总共收集到的气体的总体积为___________L(换算成标准状况下的体积)。

5、选择题 在下图装置中,若通电一段时间后乙装置左侧电极质量增加,则下列说法错误的是

甲 乙 丙
A.当甲装置中共产生标准状况下4.48 L气体时,Cu电极上质量增加43.2g
B.电解过程中装置丙的pH无变化
C.向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态
D.乙中左侧电极反应式:Cu2++2e-=Cu