1、选择题 下列叙述正确的是
A.CO有较强的还原性
B.CO2有较强的氧化性
C.SnCl2的还原性较弱
D.PbO2的氧化性较强
参考答案:AD
本题解析:CO2的氧化性很弱,Sn2+还原性较强,易被氧化成+4价,PbO2中的Pb因显+4价,易转变成较稳定的+2价,故有强的氧化性。
本题难度:简单
2、选择题 下列过程所发生的化学变化属于取代反应的是:
A.苯与液溴在FeBr3催化作用下反应
B.苯与氢气在镍做催化剂的条件下反应
C.乙烯在空气中燃烧
D.乙醇在铜做催化剂的条件下生成乙醛
参考答案:A
本题解析:有机物分子的某些原子或原子团被其它原子或原子团所代替生成其它物质的反应是取代反应,所以选项A正确。B是加成反应,CD都是氧化反应,答案选A。
本题难度:困难
3、选择题 常温下不能与铝反应的物质是
A.硫酸铜溶液
B.烧碱溶液
C.四氧化三铁
D.稀盐酸
参考答案:C
本题解析:考查铝的性质
铝做为活泼的金属,具有较强的还原性,可与酸、碱、盐发生化学反应,高温下也可与一些氧化物发生铝热反应,例如四氧化三铁,故答案为C
本题难度:困难
4、选择题 向含0.2molAlCl3的溶液中加入了一定量的1mol/L的NaOH溶液后,生成了7.8克的沉淀,则加入的NaOH溶液的体积为
A.100ml
B.200ml
C.300ml
D.400ml
参考答案:C
本题解析:析:0.2molAlCl3的溶液中加入了一定量的1mol/L的NaOH溶液后,可能发生Al3++3OH-=Al(OH)3↓,
Al(OH)3+OH-=AlO2-+2H2O,根据AlCl3的物质的量和沉淀的物质的量进行计算.
解答:解:n(Al(OH)3)=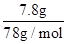 =0.1mol,而AlCl3的物质的量为0.2mol,则说明AlCl3并没有全部生成沉淀,可能有两种情况:
=0.1mol,而AlCl3的物质的量为0.2mol,则说明AlCl3并没有全部生成沉淀,可能有两种情况:
(1)NaOH不足:
Al3++3OH-=Al(OH)3↓
3mol? 1mol
n? 0.1mol
n=0.3mol,V(NaOH)=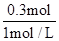 =0.3L=300ml;
=0.3L=300ml;
(2)NaOH过量
Al3++3OH-=Al(OH)3↓
1mol? 3mol? 1mol
0.2mol 0.6mol 0.2mol
Al(OH)3+OH-=AlO2-+2H2O
0.1mol? 0.1mol
共需n(NaOH)=0.6mol+0.1mol=0.7mol
V(NaOH)=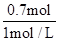 =0.7L=700ml,
=0.7L=700ml,
所以加入的NaOH溶液的体积可能为300ml或700ml,
故选C.
本题难度:简单
5、选择题 下列氧化还原反应中,同一元素既被氧化又被还原的是
A.2NO+O2====2NO2
B.N2+O2====2NO
C.N2+3H2====2NH3
D.3NO2+H2O====2HNO3+NO
参考答案:D
本题解析:同一元素既被氧化又被还原,表现为这种元素的化合价既升高又降低,标出化合价即可判定。
本题难度:困难