1��ѡ���� 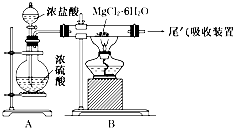 ��ͼ��ʵ������ȡ��ˮ�Ȼ�þ��װ��ͼ�������йر�����ȷ����
��ͼ��ʵ������ȡ��ˮ�Ȼ�þ��װ��ͼ�������йر�����ȷ����
A.װ��A��Բ����ƿ�п��Ի��ɹ���MnO2
B.���ֱ�Ӽ���MgCl2?6H2O���ܵõ���ˮ�Ȼ�þ�����õ�Mg��OH��Cl��MgO
C.β�����տ�����Ũ������Ϊ���ռ���������
D.����þ�ڿ�����ȼ�գ����ҷ�Ӧ��������þ���������þȼ�շ������֣�Ҫ�����ö�����̼������������
�ο��𰸣�B
������������������Ʊ�ԭ������HCl�Ļ����£�����MgCl2?6H2O���壬��ֹˮ�⣬�Ʊ���ˮ�Ȼ�þ��
A��װ��A�������Dz���HCl���壬ͨ��Bװ�÷�ֹþ����ˮ�⣻
B��ֱ��þ����ˮ�⣬���ܵõ���ˮ�Ȼ�þ�����ܵõ�Mg��OH��Cl��MgO��
C��ʵ��β���к���HCl��Ũ���������HCl��
D��Mg�����ڶ�����̼��ȼ�գ�
��𣺸��Ʊ�ԭ������HCl�Ļ����£�����MgCl2?6H2O���壬��ֹˮ�⣬�Ʊ���ˮ�Ȼ�þ��
A��װ��A�������Dz���HCl���壬װ��A��Բ����ƿ�п��Ի��ɹ���MnO2�����ܲ���HCl���壬��A����
B��ֱ��þ����ˮ�⣬���ܵõ���ˮ�Ȼ�þ�����ܵõ�Mg��OH��Cl��MgO����B��ȷ��
C��ʵ��β���к���HCl������Ⱦ������Ũ���������HCl��������ˮ���գ���ŵ�������C����
D��Mg�����ڶ�����̼��ȼ�գ�mgʧ�����ö�����̼�����������𣬹�D����
��ѡB��
����������ѧ����ʵ��ԭ�������⡢����ˮ�⡢MgԪ�ص��ʼ�����������ʵȣ��Ѷ��еȣ�ע�����֪ʶ���������գ�
�����Ѷȣ���
2��ѡ���� �������ӷ���ʽ������ȷ����
A.��������������ϡ�����У�Fe��OH��2+2H+�TFe2++2H2O
B.�ö��Ե缫����Ȼ�ͭ��Һ��Cu2++2Cl-Cu+Cl2��
C.����ˮ��Һ�ʼ��Ե�ԭ��S2-+2H2O?H2S��+2OH-
D.��NH4Al��SO4��2��Һ�е���Ba��OH��2��ҺʹSO42-ǡ����ȫ������2Ba2++4OH-+Al3++2SO42-�T2BaSO4��+AlO2-+2H2O
�ο��𰸣�B
���������������A��������������ϡ����������
B�����ݵ��ԭ�������ӷŵ�˳������жϣ�
C���������Ƕ�Ԫ���������ӷֲ�ˮ�⣻
D���������ӷ�Ӧ˳��Ͷ�����ϵ�����жϣ�NH4Al��SO4��2��Һ�е���Ba��OH��2��ҺʹSO42-ǡ����ȫ�������ʷ���1��2��Ӧ���������백����ϳ�һˮ�ϰ������ܽ����������ܽ⣻
���A����������������ϡ�����з�Ӧ������ԭ��Ӧ��3Fe��OH��2+NO3-+10H+�T3Fe3++8H2O+NO������A����
B���ö��Ե缫����Ȼ�ͭ��Һ��ͭ�����������õ���������ͭ��������������ʧ���ӷ���������Ӧ����������Cu2++2Cl- Cu+Cl2������B��ȷ��
Cu+Cl2������B��ȷ��
C������ˮ��Һ�ʼ��Ե�ԭ����������ˮ���ԭ�����ӷ���ʽ��S2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-����C����
D����NH4Al��SO4��2��Һ�е���Ba��OH��2��ҺʹSO42-ǡ����ȫ��������Ӧ˳����������ͱ����ӳ��������������Ӻ������ӳ������������������Ӻ� 笠����ӽ�ϳ�һˮ�ϰ�������ܽ�����������2Ba2++4OH-+Al3++NH4++2SO42-�T2BaSO4��+Al��OH��3��+NH3?H2O����D����
��ѡB��
���������⿼�������ӷ���ʽ�������жϺ���дԭ��ע��������ԭ��Ӧ�жϣ����ӷ�Ӧ˳���ǽ���ؼ�����Ŀ�Ѷ��еȣ�
�����Ѷȣ�����
3��ѡ���� ����Na2O?��Na2O2����������ȷ����
A.���ǰ�ɫ����
B.��Ħ��������ͬ
C.���ܺ�ˮ��Ӧ����ǿ����Һ
D.���ܺ�ˮ��Ӧ����O2
�ο��𰸣�C
���������������Na2OΪ��ɫ���壬Na2O2Ϊ����ɫ���壬���߶�����ˮ��Ӧ�������ʲ�ͬ��Na2O+H2O=2NaOH��2Na2O2+2H2O=4NaOH+O2����
���A��Na2OΪ��ɫ���壬Na2O2Ϊ����ɫ���壬��A����
B��Na2O��Ħ������Ϊ62g/mol��Na2O2��Ħ������Ϊ78g/mol�����߲�ͬ����B����
C��Na2O+H2O=2NaOH��2Na2O2+2H2O=4NaOH+O2��������NaOH����Һ�ʼ��ԣ���C��Դ:91������ www.91eXam.org��ȷ��
D��Na2O+H2O=2NaOH��û���������ɣ���D����
��ѡC��
���������⿼���ƵĻ�����֪ʶ����Ŀ�ѶȲ���ע�������ƺ���������ˮ��Ӧ�����ʣ�
�����Ѷȣ�һ��
4��ѡ���� ��������ת���ڸ��������²���ʵ�ֵ���
A.Fe2O3FeCl3��aq����ˮFeCl3
B.Al2O3NaAlO2��aq��AlCl3
C.NH3NOHNO3
D.����NaCl��aq��NaHCO3Na2CO3
�ο��𰸣�A
���������������A�������������ᷴӦ�����Ȼ�����Fe3+ˮ�⣬���������ò�����ˮFeCl3��
B�����������������Ʒ�Ӧ����ƫ�����ƣ�ƫ��������Һ�������ᣬ�����Ȼ�����
C�������Ĵ�����������һ��������һ�������ױ�����Ϊ����������������������ˮ�еõ����
D���ڱ���ʳ��ˮ��ͨ�백�����γɱ��Ͱ���ˮ����������ͨ�������̼������Һ�о����˴����������ӡ�笠����ӡ������Ӻ�̼��������ӣ�����NaHCO3�ܽ����С����������NaHCO3������NaHCO3�ֽ�����̼���ƣ�
���A�������������ᷴӦ�����Ȼ�����Fe3+ˮ��Fe3++3H2O?2Fe��OH��3+HCl����������HCl�ӷ���ƽ�������ƶ����ò�����ˮ
FeCl3����Aѡ��
B�����������������Ʒ�Ӧ����ƫ�����ƣ�ƫ��������Һ�������ᣬ�����Ȼ�������B��ѡ��
C�������Ĵ�����������һ��������һ�������ױ�����Ϊ����������������������ˮ�еõ����ᣬ��C��ѡ��
D���ڱ���ʳ��ˮ��ͨ�백�����γɱ��Ͱ���ˮ����������ͨ�������̼������Һ�о����˴����������ӡ�笠����ӡ������Ӻ�̼��������ӣ�����NaHCO3�ܽ����С������NaHCO3������NaHCO3�ֽ�����̼���ƣ���D��ѡ��
��ѡA��
���������⿼��ѧ��Ԫ�ػ���������Ƽ�������ˮ��ȷ����֪ʶ��ע��֪ʶ�����������ǽ���Ĺؼ����ѶȲ���
�����Ѷȣ�����
5��ѡ���� �������ʲ���ͨ�����Ϸ�Ӧֱ���Ƶõ���
A.FeCl2
B.NaHSO3
C.Mg(OH)2
D.Na2O2
�ο��𰸣�C
�������������þ������ˮ������������þ����ͨ�����Ϸ�Ӧ��ȡ������ǿ��Եģ���ѡC��
�����Ѷȣ���