1、选择题 某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Mg2+、Al3+、Clˉ。为确认该溶液组成进行如下实验:①取20.0 mL该溶液,加入25.0 mL 4.00? mol・L-1NaOH溶液,有白色沉淀、无剌激气味气体。过滤、洗涤、干燥,得沉淀1.16 g。再将滤液稀释至100 mL,测得滤液中c(OHˉ)为0.20 mol・L-1;②另取20.0 mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48 g。由此可得出关于原溶液组成的正确结论是
A.一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+
B.一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+
C.c (Clˉ) 为 4.00 mol・L-1,c (Al3+) 为1.00 mol・L-1
D.c (Mg2+) 为 1.00 mol・L-1,c(Na+ ) 为 0.50 mol・L-1
2、填空题 有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、 、
、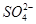 、Cl-、I-、
、Cl-、I-、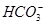 ,取该溶液进行如下实验:
,取该溶液进行如下实验:
实验步骤
| 实验现象
|
①取少量该溶液,加几滴甲基橙溶液
| 溶液变红色
|
②取少量该溶液,加入铜片和浓硫酸,加热
| 有无色气体产生,遇空气可以变成红棕色
|
③取少量该溶液,加入BaCl2溶液
| 有白色沉淀生成
|
④取③中的上层清液,加入AgNO3溶液
| 有稳定的白色沉淀生成,且不溶于稀硝酸
|
⑤取少量该溶液,加入NaOH溶液
| 有白色沉淀生成,当NaOH过量时,沉淀部分溶解
|
由此判断:
(1)溶液中一定存在的离子是?;溶液中肯定不存在的离子是?。
(2)为进一步确定其他离子,应该补充的实验及对应欲检验离子的名称(若为溶液反应,说明使用试剂的名称,不必写详细步骤)?。
(3)写出实验⑤中所有反应的离子方程式:?。
3、选择题 常温下,某溶液中由水电离产生的c(H+)与c(OH-)满足c(H+)-c(OH-)=10-24,则下列各离子组在该溶液中一定可以大量共存的是( )
A.K+Na+C6H5O-Cl-
B.Na+Cl-SO42- S2O32-
C.K+C2O42- MnO4- SO42-
D.Ba2+Na+Cl-NO3-
4、选择题 下列说法错误的是
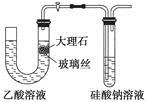
A.使用如图所示装置验证Ka(CH3COOH)>Ka(H2CO3)>Ka(H2SiO3)
B.0.1 mol・L-1的醋酸中加入水或加入冰醋酸均可使平衡向电离方向移动
C.等物质的量浓度的CH3COONa和Na2CO3溶液,后者溶液中水的电离程度大
D.等pH的醋酸和碳酸,分别加水稀释后溶液的pH仍相等,则醋酸中加入水的体积少
5、选择题 某地有甲、乙两工厂排放污水,污水中各含有下列8种离子中的4种(两厂污水不含相同的离子):Ag+、Ba2+、Fe2+、Na+、Cl-、SO42-、NO3-、OH-。若两厂污水单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便变得无色澄清,溶质主要为硝酸钠,污染程度大大降低。下列关于污染源的分析,你认为正确的是
[? ]
A.Na+和NO3-来自同一工厂
B.Cl-和NO3-一定在同一工厂
C.Ag+和Na+可能在同一工厂
D.SO42-和OH-一定来自同一工厂