|
高中化学知识点归纳《物质的量》答题技巧(2019年最新版)(八)
2019-06-28 20:41:01
【 大 中 小】
|
1、选择题 下列叙述正确的是( )
A.1 mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质体积均为22.4L
|
参考答案:C
本题解析:1 mol H2O的质量为18g,A错误;CH4的摩尔质量为16g/mol,B错误;3.01×1023个SO2分子的质量为=(3.01×1023/6.02×1023x64=32g,C正确;标准状况下,1 mol任何物质,该物质若是固体,则体积无法计算,D错误。
考点:考查化学基本概念。
本题难度:一般
2、选择题 将适量的铁粉加入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+的物质的量浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比
A.3:2
B.1:2
C.2:1
D.2:3
参考答案:D
本题解析:涉及反应为:2Fe3++Fe=3Fe2+,设原溶液中Fe3+的物质的量为a mol;参加反应的Fe3+的物质的量为bmol,则:a-b=3b/2,得:a=5b/2;
则已反应的Fe3+和未反应的Fe3+的物质的量之比:b:(a-b)=b:3b/2=2:3,答案为D
本题难度:简单
3、选择题 NA表示阿伏加德罗常数,下列说法正确的是
A.18.0 g淀粉[(C6H10O5)n]和葡萄糖混合物中共含碳原子数为0.6 NA
B.标准状况下,22.4 L己烷含有的分子数为NA
C.14g聚乙烯含有的碳原子数目为NA
D.1 mol -CH3中含有的电子数10NA
参考答案:C
本题解析:A 错误,淀粉[(C6H10O5)n]和葡萄糖最简式不同,不能计算出碳原子数
B 错误,标准状况下,己烷是液体
C 正确,碳原子数目为(14g/28n)*2nNA=NA
D 错误,1 mol -CH3中含有的电子数9NA
本题难度:一般
4、选择题 下表为四种溶液的溶质质量分数和物质的量浓度的数值,根据表中数据判断四种溶液中密度最小的是
溶液
| KOH
| HNO3
| CH3COOH
| HCl
| 溶质质量分数w(%)
| 56
| 63
| 60
| 36.5
| 物质的量浓度c(mol・L-1)
| 14.3
| 13.8
| 10.6
| 11.8
|
A.HCl B.HNO3 C.CH3COOH D.KOH
参考答案:C
本题解析:设溶液的密度为ρ(g/L),体积为V(L),溶质的摩尔质量为M(g・mol-1),则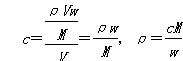 ,代入可计算出CH3COOH溶液的密度最小。 ,代入可计算出CH3COOH溶液的密度最小。
本题难度:一般
5、实验题 配制一定物质的量浓度的溶液是实验室进行科学研究的重要环节。
(1)若配制大约1 mol・L-1 的溶液100 mL,所给仪器只有托盘天平、量筒、带刻度的烧杯、玻璃棒,下列可选用的试剂是________(填字母序号)。
A.氢氧化钠固体 B.浓硫酸(98%) C.浓盐酸(37%) D.浓硝酸(63%)
(2)下图所示是某学生在配制0.100 mol・L-1 的碳酸钠溶液100 mL时,将第一次洗涤液转移到容量瓶内的操作。
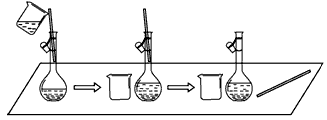
该步操作对所得溶液浓度的影响是__________(填“偏高”、“偏低”或“无影响”),原因是_____________________、___________、_____________。
(3)若配制(2)中溶液时,该生使用托盘天平称取碳酸钠,则与计算量一致吗?为什么?
____________________________________。
参考答案:(1)ABCD
(2)偏低;玻璃棒紧靠容量瓶口,造成洗涤液外溢;玻璃棒从容量瓶移出时,残留在玻璃棒上的洗涤液可能滴在瓶外;玻璃棒移出后直接放在桌面上,造成残留洗涤液损失
(3)不一致,因为碳酸钠的计算量为1.06 g,而托盘天平只能精确到0.1 g,即称取碳酸钠1.1 g
本题解析:
本题难度:一般
|