1、选择题 常温下,将一小块铝片投入足量的下列溶液中,铝片可以溶解但无氢气产生的是(?)。
A.浓盐酸
B.稀硝酸
C.氢氧化钠溶液
D.浓硝酸
参考答案:B
本题解析:硝酸是氧化性酸,和金属反应不能生成氢气。氮在浓硝酸中,铝会发生钝化,从而阻止铝和硝酸继续反应。铝既能和盐酸反应生成氢气,也能和氢氧化钠溶液反应生成氢气。所以正确的答案是B。
本题难度:一般
2、选择题 常温下不能与浓氨水形成白烟的是( )?
A.浓盐酸
B.浓硫酸?
C.浓磷酸
D.浓硝酸?
参考答案:BC?
本题解析:不能与浓氨水形成白烟的是难挥发性酸。
本题难度:简单
3、填空题 1.92gCu片与一定量的浓HNO3作用,当收集到NO2和NO气体共1.12L时(标准状况),金属铜恰好全部作用。则:
(1)反应中消耗HNO3??mol,转移电子?mol
(2)用排水法收集生成的气体,最后气体的体积为??L (标准状况)
(3)向收集到的气体中通入?mL O2(标准状况)才能使水刚好充满整个集气容器。
参考答案:⑴0.11? 0.06?⑵0.448?⑶336
本题解析:(1)根据题意知,1.92gCu片与一定量的浓HNO3作用生成硝酸铜、水、NO2和NO。根据铜原子守恒有:n[Cu(NO3)2]= n(Cu),根据氮原子守恒有:n(HNO3)=2n[Cu(NO3)2]+n(NO2+NO),则n(HNO3)=1.92g/64g・mol―1+0.05mol=0.11mol;ne=2nCu=1.92g/64g・mol―1×2=0.06mol;(2)根据题意知,n(NO)+n(NO2)=0.05mol,根据电子守恒有3n(NO)+n(NO2)=0.06mol,解得n(NO)=0.005mol,n(NO2)=0.045mol,利用排水法收集气体,发生的反应为3NO2+H2O====2HNO3+NO,收集的NO共0.02mol,标准状况下的体积为0.448L;(3)根据题意知,发生的反应为4NO+3O2+2H2O====4HNO3,n(NO) =0.02mol,则n(O2) =0.015mol,标准状况下的体积为336mL。
本题难度:一般
4、选择题 将3.84g铜粉加入到80mL lmol・L-1的稀硝酸溶液中,充分反应后,再向溶液中加入下列物质,充分搅拌后,铜粉仍然不能完全溶解的是
A.80mL l mol・L-1的稀硝酸溶液
B.80mL 0.5mol・L-1的稀盐酸
C.80mL lmnl・L-1的FeCI3溶液
D.80mL 0.5mol・L-l的稀硫酸溶液
参考答案:B
本题解析:3.84g铜粉的物质的量为0.06mol,80mL lmol・L-1的稀硝酸的物质的量为0.08mol;铜与稀硝酸反应的离子方程式为: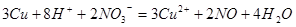 由方程式可得,铜完全溶解需氢离子物质的量为0.16mol;硝酸根离子物质的量为0.04mol,所以可得氢离子的物质的量不够,还需氢离子0.08mol;A正确,80mL l mol・L-1的稀硝酸溶液中氢离子物质的量为0.08mol;B错,80mL 0.5mol・L-1的稀盐酸中氢离子的物质的量为0.04mol;C正确,铁离子与铜反应的离子方程式为:
由方程式可得,铜完全溶解需氢离子物质的量为0.16mol;硝酸根离子物质的量为0.04mol,所以可得氢离子的物质的量不够,还需氢离子0.08mol;A正确,80mL l mol・L-1的稀硝酸溶液中氢离子物质的量为0.08mol;B错,80mL 0.5mol・L-1的稀盐酸中氢离子的物质的量为0.04mol;C正确,铁离子与铜反应的离子方程式为: ,剩余0.08mol铜需消耗铁离子的物质的量为0.06mol;80mL lmnl・L-1的FeCI3溶液中铁离子的物质的量为0.08mol;D正确,80mL 0.5mol・L-l的稀硫酸溶液氢离子的物质的量为0.08mol;
,剩余0.08mol铜需消耗铁离子的物质的量为0.06mol;80mL lmnl・L-1的FeCI3溶液中铁离子的物质的量为0.08mol;D正确,80mL 0.5mol・L-l的稀硫酸溶液氢离子的物质的量为0.08mol;
本题难度:一般
5、选择题 设空气中O2的体积分数为0.2,N2的体积分数为0.8。在有水存在的条件下,某氮的氧化物(NO与NO2形成的混合物)和一定量空气混合恰好完全反应生成硝酸,反应后气体体积减少了一半(相同条件下)。则该氮的氧化物中NO与NO2的体积比可能是
A.1∶5
B.1∶4
C.1∶3
D.任意比
参考答案:A
本题解析:
4NO? ~? 3O2
x? 0.75x
4NO2?~? O2
y? 0.25y
反应空气的体积为:(0.25y+0.75x)/0.2
反应前的混合气体体积:x+y+5(0.75x+0.25y)
反应后混合气体的体积:4(0.75x+0.25y)
于是4(0.75x+0.25y)=0.5*[x+y+5(0.75x+0.25y)],得到:y=5x,于是x:y=1:5
本题难度:一般