1、选择题 氮族元素随着核电荷数的增加,递变规律正确的是(?)
A.非金属性逐渐增强
B.熔沸点逐渐降低
C.RH3还原性逐渐增强
D.最高价氧化物对应的水化物的酸性逐渐增强
参考答案:C
本题解析:氮族元素从上至下,金属性逐渐增强,非金属性逐渐减弱;单质的熔沸点逐渐升高;氢化物的稳定性逐渐减弱,还原性逐渐增强;而最高价氧化物对应的水化物的酸性逐渐减弱。
本题难度:简单
2、选择题 已知碱能除去硝酸尾气:NO+NO2+2NaOH=2NaNO2+H2O根据硝酸尾气处理的反应原理,下列气体中不可能被过量的NaOH溶液吸收的是
A.1 mol O2和4 mol NO2
B.1 mol NO和4 mol NO2
C.1 mol O2和4 mol NO
D.4 mol NO和1 mol NO2
参考答案:D
本题解析:
本题难度:困难
3、选择题 常温常压下,将盛有20 mL NO2和O2的混合气体的大试管倒立在水槽中,水面上升至一定位置后不再变化,此时还有 3 mL气体,则原混合气体中的NO2的体积是(?)
A.17.8mL
B.14.8mL
C.13.6mL
D.12.4mL
参考答案:AC
本题解析:设NO2和O2的体积分别是x、y
x+y="20" mL ①
分两种情况:(1) 剩余O2,则NO2耗尽
4 NO2 + O2 + 2 H2O =" 4" HNO3
x? x/4
所以,y - x/4 =" 3" mL ②
联立①②,得:x =" 13.6" mL,y=" 6.4" mL,故C正确
(2) NO2过量,剩余NO
据3 NO2 + H2O =" 2" HNO3 + NO,得:NO2过量9 mL
4 NO2 + O2 + 2 H2O =" 4" HNO3
4y? y?
则:x - 4y =" 9" mL ③
联立①③,得:x =" 17.8" mL,y=" 2.2" mL,故A正确
本题难度:一般
4、选择题 下列关于过氧化氢的说法正确的是
A.过氧化氢具有杀菌消毒作用,是强酸
B.过氧化氢是离子化合物
C.过氧化氢不能发生分解反应
D.过氧化氢有漂白作用
参考答案:D
本题解析:过氧化氢不是强酸,A不正确。过氧化氢分子中含有的化学键是极性键和非极性键,所以是共价化合物,B不正确。过氧化氢不稳定,易分解生成氧气和水,C不正确。过氧化氢具有氧化性,有漂白作用,所以正确的答案选D。
本题难度:一般
5、选择题 足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68LO2(标况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至铜离子恰好完全沉淀,则消耗多少体积的NaOH是
A.60mL
B.45mL
C.30mL
D.15mL
参考答案:A
本题解析:在整个反应过程中,Cu失去电子被HNO3中N得到,使N元素化合价由+5价降低为+4、+2价;当通入1.68LO2(标况)后,化合价降低的N元素又被氧气氧化成+5价N;因此,在反应中,铜失去的电子数等于氧气得到的电子数,即,

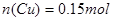
所以溶液中 ;使铜离子恰好完全沉淀需NaOH的物质的量为0.3mol;则需
;使铜离子恰好完全沉淀需NaOH的物质的量为0.3mol;则需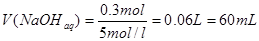
本题难度:一般