1、选择题 800 ℃时,焦炭与水蒸气反应生成一氧化碳和氢气,反应热ΔH=+131.3 kJ・mol-1,它表示
A.碳和水反应吸收热量131.3 kJ
B.固体碳和气态水各1 mol反应,放出131.3 kJ的热量
C.1 mol C跟1 mol H2O反应吸收131.3 kJ的热量
D.1 mol C(s)和1 mol H2O(g)反应生成一氧化碳和氢气,并吸收131.3 kJ的热量
参考答案:D
本题解析:考查对热化学方程式的认知
800 ℃时,C(s)+H2O(g)=CO(g)+H2(g)?ΔH=+131.3 kJ・mol-1表示, 1 mol C(s)和1 mol H2O(g)反应生成一氧化碳和氢气,并吸收131.3 kJ的热量
答案为D
本题难度:困难
2、填空题 镁与稀硝酸的反应为:Mg+ HNO3(稀)―― Mg(NO3)2+ NH4NO3+ H2O
(1)配平上述化学方程式并用“双线桥法”表示该反应中电子转移的方向和数目。
(2)该反应中,还原产物是_________,HNO3表现了________(选填“还原性”、“氧化性”、“酸性”、“碱性”)。
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为________。
参考答案:
(1) ;(2)NH4NO3;氧化性,酸性;(3)0.125 mol
;(2)NH4NO3;氧化性,酸性;(3)0.125 mol
本题解析:(1)Mg+ HNO3(稀)―― Mg(NO3)2+ NH4NO3+ H2O,Mg由0价变成了+2价化合价↑2,N由+5价变成了-3价↓8,最小公倍数是8,Mg系数×4,Mg(NO3)2系数×4,通过观察反应前后N守恒,HNO3系数×10,最后H守恒,H2O×3,得出:4Mg+10HNO3(稀)="==" 4 Mg(NO3)2+NH4NO3+3H2O;(2)N的化合价降低被还原,同时反应后NO3-的存在,因此NH4NO3是还原产物,HNO3既表现氧化性,又表现酸性;(3)HNO3→NH4NO3,生成1molNH4NO3时,共转移8mole-,现在转移了6.02×1023个电子,则被还原的硝酸的物质的量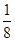 mol=0.125mol。
mol=0.125mol。
考点:考查氧化还原反应电子转移的表示方法、化学方程式的配平及计算。
本题难度:一般
3、选择题 化学反应中旧键断裂需要(?)能量
A.吸收
B.放出
C.不吸收也不放出
D.不一定
参考答案:A
本题解析:断裂化学键一定是吸收能量的,形成化学键一定放出能量。答案选A。
本题难度:一般
4、选择题 油脂水解的产物是
A.酸和甘油
B.氨基酸
C.CO2
D.水和CO2
参考答案:A
本题解析:
油脂是高级脂肪酸和甘油形成的酯类物质,酸性水解的产物是油脂是高级脂肪酸和甘油,所以选A。氨基酸是蛋白质水解的产物。水和二氧化碳一般是有机物燃烧的产物。
本题难度:一般
5、填空题 在Cu+4HNO3 = Cu(NO3)2 + 2NO2↑+2H2O反应中,________是氧化剂;______氧化产物;当6.4gCu参加反应时,电子转移的总数为______mol。
参考答案:HNO3 Cu(NO3)2 0.2
本题解析:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O中,Cu元素的化合价升高,在反应中失去电子,N元素的化合价降低,则氧化剂为HNO3,还原产物为NO2,还原剂为Cu,氧化产物为Cu(NO3)2,1molCu参加反应,转移2mol电子,6.4g铜的物质的量为0.1mol,故转移电子数为0.2mol。故答案为:HNO3;Cu(NO3)2;0.2.
考点:氧化还原反应
本题难度:一般