|
高中化学知识点讲解《化学基本概念》高频考点强化练习(2019年最新版)(六)
2019-06-28 21:05:01
【 大 中 小】
|
1、选择题 有四种物质的量浓度相等、且都由一价阳离子A+和B+及一价阴离子X―和Y―组成的盐溶液。据测定常温下AX和BY溶液的pH=7,AY溶液的pH>7,BX溶液的pH<7。由此判断可能不水解的盐是
A.BX
B.AX
C.AY
D.BY
参考答案:B
本题解析:本题考查盐类水解。强酸强碱盐不水解,故本题关键是判断哪个选项是强酸强碱盐。由AY溶液pH>7知A是强碱阳离子,Y是弱酸阴离子;BX溶液pH<7知X应是强酸阴离子,而B为弱碱阳离子;AX为强酸强碱盐,故不水解的盐应是AX。
本题难度:一般
2、选择题 下列有关氧化还原反应说法正确的是
A.工业制硫酸、工业制硝酸、由石英获取单晶硅全程变化均为氧化还原反应
B.氧化反应与还原反应一定同时发生,但氧化剂、还原剂可不直接接触
C.置换反应肯定都是氧化还原反应,但复分解反应可能是氧化还原反应
D.氧化还原反应中氧化产物与还原产物不会再发生氧化还原反应
|
参考答案:B
本题解析:A、工业制硫酸中,SO3+H2O=H2SO4的反应不是氧化还原反应,故A错误;B、氧化反应与还原反应一定同时发生,但氧化剂、还原剂可不直接接触,如原电池反应和电解反应,故B正确;C、置换反应肯定都是氧化还原反应,但复分解反应一定不是氧化还原反应,故C错误;D、属于可逆反应的氧化还原反应,氧化产物与还原产物可以发生氧化还原反应,故D错误。
考点:本题考查氧化还原反应原理。
本题难度:一般
3、选择题 常温条件,下列溶液的有关说法正确的是
A.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
B.0.1 mol/L的NH4Cl溶液中:c(NH4+) = c(Cl-)
C.同为0.1 mol/L的硫酸和氨水等体积混合后:c(NH4+) + 2c(NH3・H2O) = 2c(SO42-)
D.pH=3的盐酸和pH=11的氨水等体积混合后:c(OH-) = c(H+)
参考答案:A
本题解析:试题分析:pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,由于醋酸为弱酸,所以醋酸的物质的量远远大于NaOH溶液,所以该混合溶液呈酸性,故滴入石蕊溶液呈红色,所以A正确,为本题的选项;NH4Cl为强酸弱碱盐,所以其水溶液由于水解呈酸性,根据电荷守恒可以知道,c(NH4+) < c(Cl-),故B错误;同为0.1 mol/L的硫酸和氨水等体积混合后,根据物料守恒可以知道c(NH4+) + c(NH3・H2O) = c(SO42-),故C错误;pH=3的盐酸和pH=11的氨水等体积混合,由于一水合氨为弱碱,所以一水合氨的物质的量远远大于HCl的物质的量,故混合后溶液为碱性,所以c(OH-)> c(H+),故D不正确。
考点:盐类水解
点评:本题考查了盐类水解,该知识点是高考考查的重点和难度,本题有一定的综合性,该题难度适中。
本题难度:简单
4、选择题 除去下列溶液中的杂质(括号内为杂质),选择试剂不正确的是
A.HNO3(HCl)---用AgNO3
B.NaOH(Ba(OH)2)---用Na2SO4
C.NaCl(Na2SO4)---用Ba(NO3)2
D.KOH(K2CO3)---用Ca(OH)2
参考答案:C
本题解析:分析:除杂的方法是将杂质以沉淀或气体的形式除去;除杂的原则是所选试剂只与杂质反应,且不混入新杂质.
解答:A、盐酸和硝酸反应生成氯化银沉淀和硝酸,可以将硝酸中的盐酸出去,故A正确;
B、Ba(OH)2可以和Na2SO4反应生成硫酸钡沉淀和氢氧化钠,可以将氢氧化钠中的氢氧化钡除去,故B正确;
C、Na2SO4可以和Ba(NO3)2反应生成硫酸钡沉淀和硝酸钠,这样在氯化钠中引入了硝酸钠杂质,故C错误;
D、K2CO3可以和Ca(OH)2反应生成碳酸钙沉淀和氢氧化钾,可以将氢氧化钾中的碳酸钾除去,故D正确.
故选C.
点评:在解此类物质的除杂题时,首先分析杂质和物质性质的不同,然后选择适当的试剂和方法,只与杂质反应,不与物质反应,也不会引入新的杂质,除杂时生成物和所用试剂都不能和主要成分的状态相同,以免引入新的杂质.
本题难度:一般
5、选择题 金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为
aTiO2 + bCl2+eC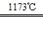 aTiCl4+eCO Ⅰ aTiCl4+eCO Ⅰ
TiCl4+2Mg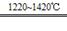 Ti+2MgCl2 Ⅱ Ti+2MgCl2 Ⅱ
关于反应Ⅰ、Ⅱ的分析不正确的是
①TiCl4在反应Ⅰ中是还原产物,在反应Ⅱ中是氧化剂;②C、Mg在两个反应中均被还原;
③在反应Ⅰ、Ⅱ中Mg的还原性大于C,C的还原性大于TiCl4;
④a=1,b="e" =2 ⑤每生成19.2 g Ti,反应Ⅰ、Ⅱ中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②③⑤
参考答案:D
本题解析:①aTiO2+bCl2+eC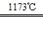 aTiCl4+eCO 该反应中反应前后,碳元素的化合价升高,碳单质作还原剂,氯元素的化合价降低,氯气作氧化剂,还原产物是TiCl4;TiCl4+2Mg aTiCl4+eCO 该反应中反应前后,碳元素的化合价升高,碳单质作还原剂,氯元素的化合价降低,氯气作氧化剂,还原产物是TiCl4;TiCl4+2Mg Ti+2MgCl2该反应中钛元素的化合价降低,TiCl4作氧化剂;所以TiCl4在反应I中是还原产物,在反应II中是氧化剂,故正确;②C、Mg在反应中反应前后化合价都升高,所以均为还原剂,被氧化,故错误;③在反应I中碳不能还原TiO2,反应II中Mg能还原TiCl4,所以镁的还原性大于C;在反应I中碳作还原剂,TiCl4作还原产物,还原剂的还原性大于还原产物的还原性,所以C的还原性大于TiCl4,故正确;④根据反应前后各元素的原子个数守恒知,2a=e、2b=4a所以a=1、b=e=2,故正确;⑤将方程式Ⅰ、Ⅱ相加得 Ti+2MgCl2该反应中钛元素的化合价降低,TiCl4作氧化剂;所以TiCl4在反应I中是还原产物,在反应II中是氧化剂,故正确;②C、Mg在反应中反应前后化合价都升高,所以均为还原剂,被氧化,故错误;③在反应I中碳不能还原TiO2,反应II中Mg能还原TiCl4,所以镁的还原性大于C;在反应I中碳作还原剂,TiCl4作还原产物,还原剂的还原性大于还原产物的还原性,所以C的还原性大于TiCl4,故正确;④根据反应前后各元素的原子个数守恒知,2a=e、2b=4a所以a=1、b=e=2,故正确;⑤将方程式Ⅰ、Ⅱ相加得
TiO2+2Cl2+2C+2Mg=Ti+2CO+2MgCl2 转移电子
48g 8mol
19.2g 3.2mol
所以每生成19.2 g Ti,反应I、II中共转移3.2 mol e-,故错误,故选D。
考点:考查氧化还原反应的有关判断与计算
本题难度:一般
|