| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《原电池原理》试题特训(2019年最新版)(二)
③在3min时该反应的平衡常数K= (计算结果) ④在图中画出8~12min之间c(CH3OH)曲线 (2)2009年,中国在甲醇燃料电池技术上获得突破,组装了自呼吸电池及主动式电堆,其装置原理如图甲。 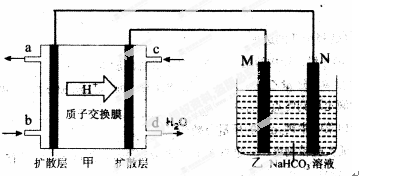 ①该电池的负极反应式为: 。 ②乙池是一铝制品表面“钝化”装置,两极分别为铝制品和石墨。 M电极的材料是 ,该铝制品表面“钝化”时的反应式为: 。 参考答案:化学反应式或方程式未配平的均扣1分 本题解析:(1)先写出三种物质的燃烧热的热化学方程式。 本题难度:困难 3、选择题 下图所示的锂离子电池主要利用碳的还原和氧化进行工作,比传统的镉镍电池、氢镍电池性能更优越。则下列叙述正确的是 参考答案:B 本题解析: 本题难度:一般 4、选择题 某温度下,体积一定的密闭容器中进行反应:N2(g)+3H2(g) 参考答案:C 本题解析:略 本题难度:一般 5、选择题 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电池的说法正确的是 参考答案:A 本题解析:试题分析:根据原电池的工作原理可知,负极电极反应式2H2-4 e-=4H+,正极电极反应式为O2+4H++4e-=2H2O,正负极电极反应式相加得电池反应式2H2+O2=2H2O,故A正确;氢氧燃料电池中,通入氢气的一极为电源的负极,所以电极a是负极,故B错误;氢氧燃料电池中,通入氧气的一极为电源的正极,发生还原反应,外电路中电子由电极a通过导线流向电极b,故C错误;氢氧燃料电池中是把化学能转化为电能,故D错误,答案选A。 本题难度:简单 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点大全《元素周期律.. | |