1、选择题 用物质的量都是0.1mol的CH3COOH和CH3COONa配制成1L混合液,其中c(CH3COO-)大于c(Na+),该混合物溶液的下列判断正确的是()
A.c(H+)>c(OH-)
B.c(CH3COOH)+c(CH3COO-)=0.2mol・L-1
C.c(CH3COOH)>c(CH3CO1O-)
D.c(CH3COO-)+c(OH-)=0.1mol・L-1
参考答案:AB
本题解析:c(CH3COO-)>c(Na+),说明CH3COOH的电离程度>CH3COO-的水解程度。因此,溶液呈酸性。A对,C错。至于B,用碳原子数守恒可证明正确。D用电荷守恒可判定不正确。
本题难度:简单
2、选择题 下列离子反应方程式中,属于水解反应的是
A.CN-+H2O HCN+OH-
HCN+OH-
B.NH3・H2O NH4++OH-
NH4++OH-
C.HCO3-+H2O H3O++CO32-
H3O++CO32-
D.H2CO3 HCO3-+H+
HCO3-+H+
参考答案:A
本题解析:
正确答案:A
B、电离;C、电离;D、电离。
本题难度:一般
3、选择题 在温度相同、浓度相同的条件下,下列六种物质的水溶液的pH由小到大的排列顺序如图所示。
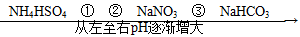
图中①②③可能是( )
A.NH4NO3、(NH4)2SO4、CH3COONa
B.(NH4)2SO4、NH4Cl、C6H5ONa
C.(NH4)2SO4、NH4NO3、Na2CO3
D.(NH4)2SO4、NH4NO3、CH3COONa
参考答案:D
本题解析:(NH4)2SO4溶液中c(NH4+)是NH4NO3溶液中c(NH4+)的2倍,所以(NH4)2SO4溶液中的酸性较强,(NH4)2SO4溶液的pH比NH4NO3溶液的小,A项不符合题意;酸性CH3COOH>H2CO3>  ?>HCO3―,所以同浓度的盐溶液,其pH大小顺序为
?>HCO3―,所以同浓度的盐溶液,其pH大小顺序为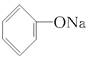 >Na2CO3>NaHCO3>CH3COONa,所以D项符合题意。
>Na2CO3>NaHCO3>CH3COONa,所以D项符合题意。
本题难度:一般
4、选择题 在相同物质的量浓度的下列盐溶液中,c(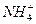 )最大的是()
)最大的是()
A.NH4HSO4
B.NH4HCO3
C.CH3COONH
D.NH4Cl
参考答案:A
本题解析:四种盐溶液中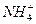 发生水解:
发生水解: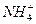 +H2O
+H2O NH3・H2O+H+,在NH4HSO4溶液中,
NH3・H2O+H+,在NH4HSO4溶液中,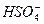 ====H++
====H++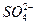 ,电离出的H+抑制了
,电离出的H+抑制了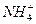 的水解;而在NH4HCO3和CH3COONH4溶液中,
的水解;而在NH4HCO3和CH3COONH4溶液中,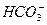 和CH3COO-也会发生水解,它们与
和CH3COO-也会发生水解,它们与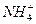 的水解是互相促进的,这样使c(
的水解是互相促进的,这样使c(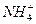 )减小。NH4Cl水溶液中
)减小。NH4Cl水溶液中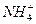 的水解既没有促进也没有抑制。显然,NH4HSO4溶液中c(
的水解既没有促进也没有抑制。显然,NH4HSO4溶液中c(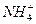 )最大。
)最大。
本题难度:简单
5、选择题 将氯化铝溶液蒸干并灼烧后得到纯净的固体A,将A在高温下熔融后用铂电极进行电解,下列有关电极产物的判断正确的是
A.阴极产物是氢气
B.阳极产物是氧气
C.阴极产物是铝和氧气
D.阳极产物只有氯气
参考答案:B
本题解析:氯化铝是强酸弱碱盐,在溶液中发生水解反应:AlCl3+3H2O Al(OH)3+3HCl。水解反应是吸热反应。所以在加热时促进了盐的水解,产生更多的反应Al(OH)3和HCl。由于HCl有挥发性,不断随着水分的蒸发而挥发,使平衡向水解的方向移动。当将氯化铝溶液蒸干得到的固体为Al(OH)3.灼烧发生分解反应2Al(OH)3
Al(OH)3+3HCl。水解反应是吸热反应。所以在加热时促进了盐的水解,产生更多的反应Al(OH)3和HCl。由于HCl有挥发性,不断随着水分的蒸发而挥发,使平衡向水解的方向移动。当将氯化铝溶液蒸干得到的固体为Al(OH)3.灼烧发生分解反应2Al(OH)3 Al2O3+3H2O。得到纯净的固体A是Al2O3。将Al2O3在高温下熔融后用铂电极进行电解,阳极发生氧化反应得到O2,阴极发生还原反应Al单质。总反应方程式为2Al2O3
Al2O3+3H2O。得到纯净的固体A是Al2O3。将Al2O3在高温下熔融后用铂电极进行电解,阳极发生氧化反应得到O2,阴极发生还原反应Al单质。总反应方程式为2Al2O3 4Al+ 3O2↑。因此正确选项为B.
4Al+ 3O2↑。因此正确选项为B.
本题难度:一般