1��ѡ���� �ں��������£���ʹCH3COONa��ϡ��Һ��c(CH3COO��)/c(Na��)��ֵ��������Һ�м����������������е�(? )
�ٹ���NaOH���ڹ���KOH���۹���NaHS���ܹ���CH3COONa���ݱ�����
A��ֻ�Т٢�
B��ֻ�Тۢ�
C��ֻ�Тڢܢ�
D��ֻ�Т٢�
�ο��𰸣�C
���������CH3COONa��Һ�д��ڣ�CH3COO����H2O?CH3COOH��OH�����������KOH�����������ʹƽ�����ƣ�c(CH3COO��)���ӹ���CH3COONa��ƽ�������ƣ���ˮ��̶Ƚ��ͣ��ڢܢݾ���ȷ��
�����Ѷȣ�һ��
2��ѡ���� Ϊ����NH4+��Ũ����Cl����Ũ�ȱ�Ϊ1��1����Һ������NH4Cl��Һ�м��루?��
�� ����HCl?�� ����NaCl?�� ������ˮ?�� ����NaOH
A���٢�
B����
C���ۢ�
D����
�ο��𰸣�B
����������٢������Լ������Һ����������,ʹ������Ũ������.��������е�NaOH����NH4+��Ӧ����NH3��H2O,ʹNH4+Ũ�ȼ�С.����Ӧ��ѡB.
�����Ѷȣ�һ��
3��ѡ���� ����ʵ��Ӧ�����ε�ˮ��֪ʶ�ص���
A������ʱ��NH4Cl��Һ����
B����ĭ����������������뱥��С�մ���Һ
C�������Ȼ�����Һ�����ˮ�Ʊ�Fe(OH)3����
D�������е��ʳ��ˮ��ȡ����Һ
�ο��𰸣�D
���������A��ȷ��笠�����ˮ��ʹ��Һ�����ԣ������������������Һ�С�
B��ȷ�������Ӻ�̼���������˫ˮ�⡣
C��ȷ��������ˮ�⡣
D�����Ȼ��Ʋ�ˮ�⣬�������ӵ�Դ�����µ�������ԭ��Ӧ����ѡD
�����Ѷȣ���
4������� (15��)��ˮ�и���þ���ɾ����Ӽ���������ˡ����ܡ��ᾧ����ˮ�Ȳ���õ���ˮ�Ȼ�þ��
�����õ�����þ��
��1���Ӽ����þ����ʱ�����ɵ�Mg(OH)2�ڷ�ɢϵ�д��ڳ����ܽ�ƽ�⣬���ܶȻ���������ʽ
Ksp=?��
��2��MgCl2��Һ�����ԣ���ˮ������ӷ���ʽΪ?��
��3����ȥMgCl2������Һ��������FeCl3���ɼ�����Լ���?
a��MgO? b��Mg(OH)2? c��MgCO3? d��MgSO4
��4�����ڿ����м���MgCl2��6H2O��������Mg(OH)Cl��MgO��д����صĻ�ѧ����ʽ֮һ
?��
��5��MgCl2��6H2O�ڸ����HCl�����м��ȿɵõ���ˮ�Ȼ�þ����ԭ����?��
��6��������ڵ�MgCl2�������ĵ缫��ӦʽΪ��?�������ĵ缫��ӦʽΪ?��
�ο��𰸣���1��Ksp=c(Mg2+)��c2(OH��) ��3�֣�
��2��Mg2+ + 2H2O  ?Mg(OH)2 +2H+��2�֣�
?Mg(OH)2 +2H+��2�֣�
��3��abc��2�֣�
��4��MgCl2��6H2O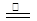 Mg(OH)Cl + HCl��+5H2O����MgCl2��6H2O
Mg(OH)Cl + HCl��+5H2O����MgCl2��6H2O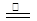 MgO + 2HCl��+5H2O����2�֣�
MgO + 2HCl��+5H2O����2�֣�
��5��HCl����������Mg2+ˮ�⣨2�֣�
��6��2Cl�D�D2e��=Cl2����2�֣���Mg2++2e��=Mg��2�֣�
����������Ÿ���Mg(OH)2���ܽ�ƽ��ʽ��Mg(OH)2(s) Mg2+(aq)+2OH- (aq)��д�����ܶȻ���������ʽ��
Mg2+(aq)+2OH- (aq)��д�����ܶȻ���������ʽ��
��MgCl2��Һ��Mg2+ˮ�⣺Mg2+ + 2H2O  ?Mg(OH)2 +2H+��ʹ��Һ�����ԣ�
?Mg(OH)2 +2H+��ʹ��Һ�����ԣ�
�Ǹ���FeCl3��ˮ�⣺FeCl3+3H2O Fe(OH)3+3HCl������MgO��Mg(OH)2��MgCO3���ܴٽ�FeCl3��ˮ�⣬ʹ��ת��Fe(OH)3��������ȥ��ͬʱ������MgO��Mg(OH)2��MgCO3��ͨ�����˳�ȥ��
Fe(OH)3+3HCl������MgO��Mg(OH)2��MgCO3���ܴٽ�FeCl3��ˮ�⣬ʹ��ת��Fe(OH)3��������ȥ��ͬʱ������MgO��Mg(OH)2��MgCO3��ͨ�����˳�ȥ��
���ڿ����м���MgCl2��6H2O���ٽ�MgCl2��ˮ�⣬��HCl��H2O�ݳ���������Mg(OH)Clʱ�䷴Ӧ����ʽΪMgCl2��6H2O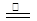 Mg(OH)Cl + HCl��+5H2O����������MgOʱ�䷴Ӧ����ʽΪMgCl2��6H2O
Mg(OH)Cl + HCl��+5H2O����������MgOʱ�䷴Ӧ����ʽΪMgCl2��6H2O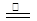 MgO + 2HCl��+5H2O����
MgO + 2HCl��+5H2O����
��MgCl2��6H2O�ڸ����HCl�����м��ȣ�HCl����������Mg2+ˮ�⣬�����ɵõ���ˮ�Ȼ�þ��
�ʵ�����ڵ�MgCl2����������������Ӧ����缫��ӦʽΪ2Cl�D�D2e��=Cl2��������������ԭ��Ӧ����缫��ӦʽΪMg2++2e��=Mg��
�����Ѷȣ�һ��
5��ѡ���� Ϊ��֤��ԭ�Ե�������ˮ�⣬��ˮ�����������л�ԭ�ԣ�����������ʵ�鲽�裺�ټ���ϡ����ڼ��뼸��CuSO4���ۼ��ȣ��ܼ�������ˮ���ݼ����ռ���Һ�����ԣ���������Cu��OH��2����Һ�����˳��
A���ܢ٢ۢޢ�
B���ܢۢ٢ޢݢ�
C���٢ۢڢޢ�
D���ܢ٢ۢݢޢ�
�ο��𰸣�D
�������������ˮ���ϲ������Ǻ��ǡ����ں����Ƶ�������ͭ����Һ��Ӧ����Ҫ�ڼ��������½��У���������Ҫ������������֮�����ᣬ�����ȷ�Ĵ�ѡD��
�����Ѷȣ���