1、简答题 1,2,3,4-四氢化萘的结构简式如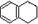 ,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2→C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2→C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:

①按一定质量比把四氢化萘和水加入适当的容器中,加入少量纯铁粉.
②慢慢滴入液溴,不断搅拌,直到反应完全.
③取下反应容器,补充少量四氢化萘,直到溶液颜色消失.过滤,将滤液倒入分液漏斗,静置.
④分液,得到的“水层”即氢溴酸溶液.回答下列问题:
(1)如右图所示的装置,适合步骤①和②的操作的是______;
(2)步骤③中补充少量四氢化萘的目的是______;
(3)步骤③中过滤后得到的固体物质是______.
(4)在④获得的浓溶液中加入乙醇并加热,可获得一种不溶于水的有机物,写出该反应的方程式______;实验室制取乙炔可用上图中的装置D,这时分液漏斗中的液体通常是______.
(5)乙炔能被酸性高锰酸钾溶液氧化,请配平其相应的方程式:
______C2H2+______KMnO4+______H2SO4=______K2SO4+______MnSO4+______CO2+______H2O.
参考答案:(1)按照步骤①,本实验是把四氢化萘、水和铁粉加入同一容器中反应,所以B不正确.若用A中的装置进行反应,溴蒸气和刺激性气味的四氢化萘都会污染环境,同样C装置在步骤②反应时,也会造成环境污染,所以A、C都不对,故选D装置,
故答案为:D;
(2)由于步骤②加入了过量的液溴,步骤③中补充少量四氢化萘除掉剩余的溴单质,
故答案为:反应掉多余的Br2;
(3)由于生成的四溴化萘常温下为固态,所以过滤后得到的固体物质是四溴化萘和铁粉,
故答案为:四溴化萘和铁粉;
(4)在④获得的浓溶液中含有溴化氢,溴化氢与乙醇在加热条件下生成溴乙烷,反应的方程式为:CH3CH2OH+HBr△
本题解析:
本题难度:一般
2、选择题 限用下列一种试剂鉴别氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,这种试剂是( )
A.KSCN
B.HCl
C.BaCl2
D.NaOH
参考答案:取五种溶液分别滴加NaOH溶液时,产生白色沉淀的是氯化镁;先产生沉淀,后沉淀溶解的是氯化铝;产生红褐色沉淀的是氯化铁;产生白色沉淀,后又变灰绿色,最后变成红褐色的是氯化亚铁;无现象的是氯化钠,而加入KSCN只能检验氯化铁,加入盐酸和氯化钡不能检验任何物质,
故选D.
本题解析:
本题难度:一般
3、选择题 下列相关实验不能达到预期目的的是
?
| 相关实验
| 预期目的
|
A.
相同温度下,等质量的大理石块、大理石粉分别与等体积、等浓度的盐酸反应
探究接触面积对化学反应速率的影响
B.
把装有颜色相同的NO2和N2O4混合气的两支试管(密封)分别浸入冷水和热水中
探究温度对化学平衡的影响
C.
在蔗糖中加入稀硫酸,水浴加热,再加入新制的氢氧化铜并加热
探究蔗糖水解产物具有还原性
D.
两支试管中装有等体积、等浓度H2O2溶液,向其中一支试管中加入FeCl3溶液
探究FeCl3溶液对H2O2分解速率的影响
|
题型:单选题难度:中档来源:不详 答案 蔗糖在稀H2SO4溶液水解后应加入NaOH溶液中和掉H2SO4使溶液呈碱性,否则加入新制Cu(OH)2并加热时,得不到Cu2O沉淀,也无法探究蔗糖水解产物具有还原性。
马上分享给同学