1、选择题 下列有关电池的说法不正确的是
[? ]
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
参考答案:B
本题解析:
本题难度:一般
2、填空题 甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ: CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
温度
| 250℃
| 300℃
| 350℃
|
K
| 2.041
| 0.270
| 0.012
|
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
②某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH1=-1451.6kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2=-566.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:

①该电池的能量转化形式为 。
②该电池正极的电极反应为 。
③工作一段时间后,测得溶液的pH减小,则该电池总反应的化学方程式为 。
参考答案:(1)①<(2分) ②80%(2分) 250℃(2分)
(2)CH3OH(l) + O2(g) = CO(g) + 2H2O(l) ΔH1=-442.8kJ/mol(3分)
⑶①化学能转化为电能(2分)
②O2 + 2H2O +4e- = 4OH-(2分)
③2CH3OH + 3O2 + 4OH-= 2CO32-+ 6H2O(3分
本题解析:(1)①由题给数据分析,随着温度的升高,平衡常数减小,平衡向逆向移动,升温平衡向吸热方向移动,该反应正向为放热反应,ΔH1<0;②利用三行式进行计算。按反应II充分反应,达到平衡后,测得c(CO)=0.2mol/L,设转化的CO的物质的量浓度为x,
CO(g)+2H2 (g) CH3OH (g)
CH3OH (g)
起始量(mol/L) 1 3 0
变化量(mol/L) x 2x x
平衡量(mol/L) 0.2 3-2x x
分析知x=0.8mol/L
平衡时各物质的浓度:c(CO)=0.2mol/L,c(H2)=1.4mol/L,c(CH3OH)=0.8mol/L;一氧化碳的转化率=0.8/1×100%=80%,K=0.8/0.2×1.42=2.041,由表格可知温度为250℃;(2)由盖斯定律,①-②得:2CH3OH(l)+2O2(g)
本题难度:困难
3、选择题 如图所示装置,电流计的指针发生偏转,正极变粗,负极变细,符合这种情况的是
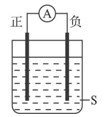
A.正极Cu,负极Al,S为浓HNO3
B.正极Ag,负极Fe,S为CuSO4
C.正极Al,负极Cu,S为浓HNO3
D.正极Zn,负极Cu,S为CuSO4
参考答案:B
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。由于在该装置中正极变粗,负极变细,这说明溶液中金属阳离子在正极得到电子而析出,所以只有选项B是正确的,其余选项都是错误的,答案选B。
本题难度:一般
4、选择题 由铝,铁,铜,银和稀硫酸,可以组成原电池的总数为( )
A.3种
B.4种
C.5种
D.6种
参考答案:铝,铁,铜,银这四种金属的活泼性不同,但能和稀硫酸自发的进行氧化还原反应的金属有铝和铁,所以负极材料必须含有铝或铁中的一种,
则以下几种情况的电极与稀硫酸可组成的原电池有①铝和铁、②铝和铜、③铝和银、④铁和铜、⑤铁和银,
所以组成原电池的总数为5种,
故选C.
本题解析:
本题难度:简单
5、选择题 瑞典ASES公司设计的用于驱动潜艇的液氨-液氧燃料?电池示意图如下,有关说法正确的是

A.电池总反应为:4NH3 + 3O2 = N2 + 6H2O
B.电池工作时,OH-向负极移动
C.电极2发生的电极反应为:O2+4H+ + 4e-=2H2O
D.电流由电极1经外电路流向电极2
参考答案:B
本题解析:A、该化学方程式没有配平,错误;B、电池工作时,阴离子向负极移动,正确;C、该电池的电解质溶液为NaOH溶液,所以电极2发生的电极反应为:O2+2H2O+4e?=4OH?,错误;D、电流由正极流向负极,所以电流由电极2经外电路流向电极1,错误。
本题难度:一般