1ЎўСЎФсМв іЈОВПВЈ¬ПВБР¶ФУР№ШИЬТєµДЕР¶ПІ»ХэИ·µДКЗЈЁ?Ј©
AЈ®Na2CO3ИЬТєЦРЈ¬c(OH-) = c(H+)Ј«c(HCO3ЁC)Ј«c(H2CO3)
BЈ®ОВ¶ИПаН¬ЎўЕЁ¶ИПаН¬µДўЩ(NH4)2SO4ЎўўЪNaNO3ЎўўЫNH4HSO4ЎўўЬNH4NO3ЎўўЭ ЎўўЮCH3COONaИЬТєЈ¬ЛьГЗµДpHЦµУЙРЎµЅґуµДЕЕБРЛіРтКЗЈєўЫўЩўЬўЪўЮўЭ
ЎўўЮCH3COONaИЬТєЈ¬ЛьГЗµДpHЦµУЙРЎµЅґуµДЕЕБРЛіРтКЗЈєўЫўЩўЬўЪўЮўЭ
CЈ®NaAИЬТєµДpHЈЅ8Ј¬c(Na+)Јc(A-) = 0.99ЎБ10-6 mol/L
DЈ®10 mL pH = 12µДЗвСх»ЇДЖИЬТєЦРјУИлpH = 2µДHAЦБpHёХєГµИУЪ7Ј¬ЛщµГИЬТєМе»эV(ЧЬ)ЎЬ20mL
2ЎўСЎФсМв іЈОВК±Ј¬Ѕ«V1mL c1molЎ¤LЈ1µД°±Л®µОјУµЅV2mL c2moLЎ¤LЈ1µДСОЛбЦРЈ¬ПВБРЅбВЫЦРХэИ·µДКЗ
AЈ®Иф»мєПИЬТєµДpH=7Ј¬Фтc1V1Јѕc2V2
BЈ®ИфV1=V2Ј¬c1=c2Ј¬ФтИЬТєЦРc (NH4+) =c (Cl-)
CЈ®Иф»мєПИЬТєµДpH=7Ј¬ФтИЬТєЦРc (NH4+)Јѕc (Cl-)
DЈ®ИфV1=V2Ј¬ЗТ»мєПТєµДpHЈј7Ј¬ФтїЙДЬУРc1 = c2
3ЎўСЎФсМв 25ЎжЈ¬101 kPaК±Ј¬ЗїЛбУлЗїјоµДПЎИЬТє·ўЙъЦРєН·ґУ¦µДЦРєНИИОЄ57.3kJЎ¤mol-1Ј¬РБНйµДИјЙХИИОЄ
5518 kJЎ¤mol-1ЎЈПВБРИИ»ЇС§·ЅіМКЅКйРґХэИ·µДКЗ
[? ]
A.2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH-(aq) =BaSO4(s)+2H2O(l), ЎчH=-114.6 kJЎ¤mol-1
B.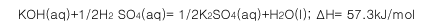
C. C8H8(l)+25/2O2(g)==8CO2+9H2O,ЎчH=-5518kJ/mol
D.2C8H18(g) +25O2(g) =16CO2(g) + 18H2O(l), ЎчH = -5518 kJЎ¤mol-1
4ЎўСЎФсМв ПВБР№ШУЪИИ»ЇС§·ґУ¦µДГиКцЦРХэИ·µДКЗ
[? ]
AЈ®ТСЦЄH+(aq)+OH-(aq)==H2O(l)Ј»ЎчHЈЅ-57.3kJЎ¤mol-1Ј¬ФтH2SO4єНBa(OH)2·ґУ¦µД·ґУ¦ИИЎчH=2ЎБ(-57.3)kJЎ¤mol-1
BЈ®ИјБПµзіШЦРЅ«јЧґјХфЖшЧЄ»ЇОЄЗвЖшµДИИ»ЇС§·ЅіМКЅКЗCH3OH(g)+1/2O2(g)==CO2(g)+2H2(g)Ј» ЎчH=-192.9 kJЎ¤mol-1Ј¬ФтCH3OHµДИјЙХИИОЄ192.9 kJЎ¤mol-1
CЈ®H2(g)µДИјЙХИИКЗ285.8 kJЎ¤mol-1Ј¬Фт2H2O(g)==2H2(g)+O2(g)Ј»ЎчH=+571.6 kJЎ¤mol-1
DЈ®ЖПМСМЗµДИјЙХИИКЗ2800 kJЎ¤mol-1Ј¬Фт1/2 C6H12O6 (s)+3O2 (g)==3CO2 (g)+3H2O ( l )Ј» ЎчH=-1400 kJЎ¤mol-1
5ЎўСЎФсМв јЧНйКЗТ»ЦЦёЯР§ЗеЅаµДРВДЬФґ,0.25 mol CH4НкИ«ИјЙХЙъіЙТєМ¬Л®К±·Еіц222.5 kJИИБї,ФтПВБРИИ»ЇС§·ЅіМКЅЦРХэИ·µДКЗ(ЎЎЎЎ)
AЈ®2CH4(g)+4O2(g) 2CO2(g)+4H2O(l)ЎЎ¦¤H="+890" kJЎ¤mol-1
2CO2(g)+4H2O(l)ЎЎ¦¤H="+890" kJЎ¤mol-1
BЈ®CH4(g)+2O2(g) CO2(g)+2H2O(l)ЎЎ¦¤H="+890" kJЎ¤mol-1
CO2(g)+2H2O(l)ЎЎ¦¤H="+890" kJЎ¤mol-1
CЈ®CH4(g)+2O2(g) CO2(g)+2H2O(l)ЎЎ¦¤H="-890" kJЎ¤mol-1
CO2(g)+2H2O(l)ЎЎ¦¤H="-890" kJЎ¤mol-1
DЈ®2CH4(g)+4O2(g) 2CO2(g)+4H2O(l)ЎЎ¦¤H="-890" kJЎ¤mol-1
2CO2(g)+4H2O(l)ЎЎ¦¤H="-890" kJЎ¤mol-1