1、实验题 (16分)食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含少量K+、Ca2+、Mg2+、Fe3+、SO42―等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液 、? 75%乙醇、四氯化碳;欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42―离子,选出a所代表的试剂,按滴加顺序依次是?(只填化学式)。
(2)用提纯的NaCl配制500 mL 4.00 mol・L-1 NaCl溶液,所用仪器除药匙、玻璃棒、托盘天平、烧杯还需要?(填仪器名称);若定容时仰视刻度线,则所配溶液的浓度?(填“偏大”、“偏小”或“无影响”)。
(3)在电解饱和食盐水的实验中,若收集的H2为3.36 L(在标准状况下),则转移电子的个数为?,同样条件下收集的Cl2?(填“>”、“=”或“<”)3.36 L。
(4)实验室制备Cl2通常采用二氧化锰与浓盐酸共热来制取,发生反应的离子方程式为:?;
据此,从下列所给仪器装置中选择制备并收集干燥、纯净Cl2的装置?(填代号)
可选用制备气体的装置:

所选装置中的两个洗气瓶里应依次盛装?、?(填试剂的名称),请结合化学平衡移动原理解释第一个洗气瓶中试剂选择的理由?;尾气用?溶液(填化学式)吸收,写出发生反应的离子方程式?。
参考答案:(16分)
(1) BaCl2、NaOH 、Na2CO3(2分,其他合理顺序也给分)
(2)500 mL的容量瓶、胶头滴管(2分,写与不写“量筒”均不扣分)
偏小(1分)
(3)0.3NA或1.806×1023(1分 )
<?(1分)?
(4)MnO2+4H++2Cl-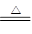 Mn2++Cl2↑+2H2O(2分 )
Mn2++Cl2↑+2H2O(2分 )
d (1分 )
饱和食盐水或饱和的氯化钠溶液、浓硫酸(2分 )
Cl2溶于水并与水发生反应Cl2 +H2O  ?H++Cl―+HClO,增大Cl―的浓度使平衡向左移动,有利于收集更多的氯气?(2分 ) NaOH (1分 ) Cl-+2OH-=Cl-+ClO-+H2O(2分 )
?H++Cl―+HClO,增大Cl―的浓度使平衡向左移动,有利于收集更多的氯气?(2分 ) NaOH (1分 ) Cl-+2OH-=Cl-+ClO-+H2O(2分 )
本题解析:略
本题难度:一般
2、填空题 (12分)已知固体草酸(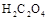 )分解的化学方程式为:
)分解的化学方程式为:
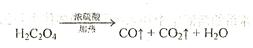
某实验小组为测定铁锈样品的组成(假定铁锈中只有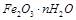 和
和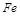 两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
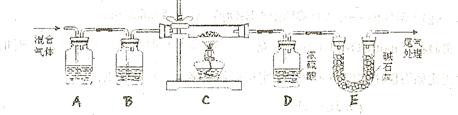
(1)为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次是?、?(填答案编号)a.浓硫酸? b.澄清的石灰水? c.氢氧化钠溶液? d.氯化钙溶液
(2)在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;
(b)??;
(3)E装置的作用是?。
上述装置最后尾气处理的方法是?:
(4)准确称量样品质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n=?.
(5)在本实验中,下列情况会使测定结果n偏大的是?(填答案编号)
a.缺少装置B? b.缺少装置E? c.反应后的固体剩余少量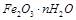
参考答案:

本题解析:(1)混合气体的主要成分为: ?、
?、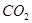 、
、 ,得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次是氢氧化钠溶液除去二氧化碳气体,浓硫酸除去水蒸气;
,得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次是氢氧化钠溶液除去二氧化碳气体,浓硫酸除去水蒸气;
(2)CO气体为可燃性气体,为防止加热时产生爆炸,加热前应通入混合气体一段时间,排净体系中的空气,再加热;
(3)装置E的作用是吸收生成的二氧化碳气体,同时防止空气中的水蒸气进入体系,影响实验结果;最后尾气处理的方法是:在装置后放一燃着的酒精灯;
(4)反应结束后,固体质量减少为10.00―8.32=1.68g;D中浓硫酸增重0.72g,即含水蒸气为0.72g;样品中氧化铁中的氧元素的质量为:1.68―0.72=0.96g;CO与其关系为
CO~O~CO2,即生成的二氧化碳的物质的量为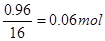 ;则由方程式:
;则由方程式:
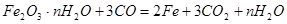
3mol? 18n g
0.06mol? 0.72g
解得n=2;
(5)ab
本题难度:一般
3、实验题 现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:
①2Mg+O2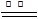 2MgO;②3Mg+N2
2MgO;②3Mg+N2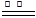 Mg3N2;③2Mg+CO2
Mg3N2;③2Mg+CO2 2MgO+C;
2MgO+C;
④Mg+H2O MgO+H2↑; ⑤Mg3N2 +6H2O
MgO+H2↑; ⑤Mg3N2 +6H2O 3Mg(OH)2+2NH3↑
3Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。
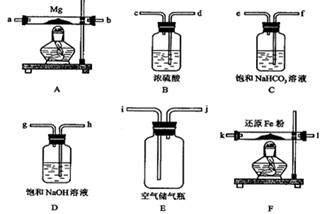
回答下列问题:
(1)在设计实验方案时,除装置A、D、E外,还应选择的装置有?(填字母代号),选择装置D目的为_____________________________?;
(2)通气后,应先点燃?处的酒精灯;如果同时点燃A、F装置的酒精灯,将会使实验结果?(填“偏高”或“偏低”)原因?
(3)请设计一个实验,验证产物是Mg3N2,写出操作步骤、现象和结论:
_____________________________________________________________________?
参考答案:(1)BF?(2分)? D 目的是除去空气中的CO2,避免反应③发生;(2分)
(2)F;(1分)偏低;(2分)如果装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧同镁反应,而使氮化镁中混入氧化镁。(2分)
(3)取适量产物放入试管中,滴加蒸馏水,将润湿的红色石蕊试纸靠近试管口,如果试管中的溶液出现浑浊,红色石蕊试纸变蓝,则可以证明有氮化镁生成。(2分)
本题解析:(1)该反应中为了得到纯净的氮化镁,必须把影响的产物的气体水,还有氧气去除,装置B是用来除去水蒸汽的,放在A之前,F可以用来除去氧气。D 目的是除去空气中的CO2,避免反应③发生;
(2)这一装置中,很多人可能会考虑到F装置是用来除去水蒸汽的,那样的话,反应产生的氢气怎么办,因此这个装置是用来除去氧气的。如果装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧同镁反应,而使氮化镁中混入氧化镁。(2分)
(3)验证产物是Mg3N2,必须利用氮化镁的特征反应。取适量产物放入试管中,滴加蒸馏水,将润湿的红色石蕊试纸靠近试管口,如果试管中的溶液出现浑浊,红色石蕊试纸变蓝,则可以证明有氮化镁生成。
本题难度:一般
4、实验题 (10分)实验室制取乙酸乙酯的主要步骤如下:
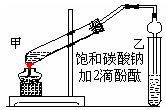
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液.
②按右图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置待分层。④分离出乙酸乙酯层、洗涤、干燥。
(1)反应中浓硫酸的作用是___________________写出制取乙酸乙酯的化学方程式:___________________________________;
(2)上述实验中饱和碳酸钠溶液的作用是(填字母):_______________。
A.中和乙酸和乙醇。
B.中和乙酸并吸收部分乙醇。
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出。
D.加速酯的生成,提高其产率。