1、填空题 有A、B、C、D、E、F六种物质,它们之间相互转化关系如图所示(条件及部分产物未标出)。
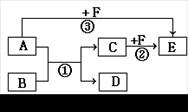
(1)若A、D为气体,都能使澄清的石灰水变浑浊;B、F做焰色反应,透过蓝色钴玻璃观察为紫色, B、C为正盐,F的溶液为紫红色。则C和F在酸性溶液中发生反应②的离子方程式为?。?
(2)若1 mol A分子中含有3 mol极性共价键, B、C、F都是短周期元素组成的非金属单质;常温下,只有D为固体,其它为气体。则反应③的化学方程式为?。?
某同学设计了如图所示装置(夹持仪器省略)进行上述(2)中物质B的化学性质探究。
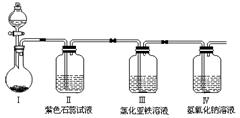
①你认为此装置设计是否合理?若不合理如何改进:?。(若合理此问不答)
②Ⅱ中产生的现象是?。
③反应几分钟后,检验Ⅲ中可能含有的金属阳离子的实验操作是?。
④通过以上探究,气体B的主要化学性质是?。
2、选择题 (2011・广东六校模拟)用下图装置进行实验,下表中实验结果能说明结论的是( )
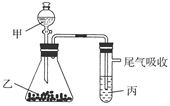
?
| 甲
| 乙
| 丙
| 结论
|
A
| 水
| 电石
| 溴水
| 稳定性:水>C2H2>Br2
|
B
| 盐酸
| 石灰石
| 苯酚钠溶液
| 酸性:HCl>H2CO3>苯酚
|
C
| 盐酸
| FeS
| 溴水
| 还原性:S2->Br->Cl-
|
D
| 浓盐酸
| KMnO4
| KBr溶液
| 氧化性:KMnO4<Cl2<Br2
|
?
3、实验题 亚铁盐中,FeSO4?7H2O露置于空气中易被氧气氧化,而莫尔盐[(NH4)2SO4?FeSO4?6H2O]露置于空气中不易被氧气氧化,是一种重要的定量分析试剂。其制备原理是:FeSO4+(NH4)2SO4+6H2O =(NH4)2SO4?FeSO4?6H2O。
实验室用废铁屑制备莫尔盐的过程如下:

(1)步骤I除锈的操作是:将废铁屑放入烧杯,?,过滤,洗涤。
(2)步骤II铁屑的溶解在锥形瓶中进行,并水浴加热到60℃左右,需要的仪器是铁架台、石棉网、大烧杯、?。
(3)步骤III中加入的(NH4)2SO4与溶液中FeSO4的物质的量需满足的关系为:n[(NH4)2SO4]∶n[FeSO4]=?。
为了确定(NH4)2SO4的用量,下列方法简便可行的是??(填编号)。
A.称量废铁屑的质量,推算所需(NH4)2SO4的质量
B.称量无锈铁屑和步骤II之后剩余铁屑的质量,推算所需(NH4)2SO4的质量
C.测定FeSO4溶液的浓度和体积,推算所需(NH4)2SO4的质量
(4)所得晶体样品中可能混有的杂质是FeSO4・7H2O和(NH4)2SO4中的一种。某小组设计了如下方案进行检验和测定,请在答题卡上完成表中内容。
序号
| 实验方案
| 实验现象和结论
|
步骤1
| 取少量样品?
| 样品颜色可能有变化。
|
步骤2
| 步骤1后将样品转移到试管中,加入去氧蒸馏水,振荡溶解,调节至酸性,________
___________? __ ?。
| 若?,说明样品中含有FeSO4・7H2O杂质。
|
步骤3
| 若步骤2证明样品不含FeSO4?7H2O杂质,再另取样品测定其中NH4+的质量分数w1与理论值w2比较。
| 若w1?w2,说明样品中含有(NH4)2SO4杂质。
|
(已知(NH4)2SO4?FeSO4?6H2O的式量为392,(NH4)2SO4的式量为132)
4、填空题 化学小组采用类似制乙酸乙酯的装置(如下图),用环己醇制备环己烯。
已知:
?
| 密度(g/cm3)
| 熔点(℃)
| 沸点(℃)
| 溶解性
|
环己醇
| 0.96
| 25
| 161
| 能溶于水
|
环己烯
| 0.81
| -103
| 83
| 难溶于水
|
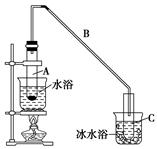
(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片(防止爆沸),缓慢加热至反应完全,在试管C内得到环己烯粗品。
①导管B除了导气外还具有的作用是________。
②试管C置于冰水浴中的目的是______________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在________层(填“上”或“下”),分液后用________(填入编号)洗涤。
A.KMnO4溶液? B.稀H2SO4?C.Na2CO3溶液

②再将环己烯按上图装置蒸馏,冷却水从________口进入(填“g”或“f”)。蒸馏时要加入生石灰,其目的是_____________________________________。
③收集产品时,控制的温度应在________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是________。
A.蒸馏时从70 ℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是________。
A.分别加入酸性高锰酸钾溶液
B.分别加入用金属钠
C.分别测定沸点
5、选择题 既不能用浓硫酸干燥,又不能用碱石灰干燥的气体是( )
A.Cl2
B.H2S
C.SO2
D.CO2