1、选择题 向纯水中加入少量下列物质或改变下列条件,能促进水的电离,并能使溶液中c(OH―) > c(H+)的操作是: ①稀硫酸?②金属钠?③氨气?④FeC13固体?⑤NaClO固体?⑥将水加热煮沸
A.②⑤
B.①④
C.③④⑥
D.④
参考答案:A
本题解析:考查影响水的电离的外界因素。盐的水解能促进水的电离,但酸或碱是抑制水的电离的,因此①③抑制。加入金属钠,和水电离出的氢离子反应生成氢氧化钠和氢气,使水的电离向右移动,碱性增强,c(H+)<c(OH-);加热促进水的电离,但水中c(OH―)=c(H+);氯化铁水解,溶液显酸性。次氯酸钠水解,溶液显碱性,所以正确的答案选A。
本题难度:一般
2、选择题 将①H+、②Cl-、③Al3+、④K+、⑤S2-、⑥OH-、⑦NO3-、⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的是
A.①③⑤⑦⑧
B.②④⑦
C.①⑥
D.②④⑥⑧
参考答案:B
本题解析:酸或碱以及能够水解的盐都会影响水的电离平衡,则①③⑤⑥⑧都影响水的电离平衡,②④⑦不会影响水的电离平衡,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生能力的培养和解题方法的指导和训练,该题的关键是明确外界条件是如何影响水的电离平衡的,有利于培养学生的逻辑推理能力,提高学生的答题能力。
本题难度:一般
3、选择题 MOH和ROH两种碱的溶液分别加水稀释时,pH变化如图所示。下列叙述中正确的是(?)
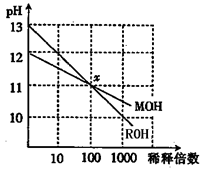
A.MOH是一种强碱
B.在x点,MOH完全电离
C.在x点,c(M+)==c(R+)
D.稀释前,c(ROH)==10c(MOH)
参考答案:C
本题解析:A.ROH是一种强碱,MOH为弱碱;
B.在x点,MOH和ROH溶液pH值相同;
D.稀释前,c(ROH中的OH-)==10c(MOH中的OH-);
本题难度:一般
4、选择题 一定温度下,满足下列条件的溶液一定呈酸性的是
A.pH=6的某溶液
B.加酚酞后显无色的溶液
C.能与金属Al反应放出H2的溶液
D.c(H+)>c(OH―)的任意水溶液
参考答案:D
本题解析:A、当温度升高时,水的离子积增大,[H+]=[OH-]=10-6mol/L,此时溶液仍呈中性,故A错误;酚酞的变色范围是8-10,小于8时溶液显无色,可能为碱性、中性或酸性,故B错误;C、能与铝作用放出氢气的可能为强酸或强碱,故C错误;溶液的酸碱性决定于氢离子和氢氧根离子浓度的相对大小,当氢离子的浓度大于氢氧根离子的浓度时,溶液一定呈酸性,D正 确;故选D。
本题难度:一般
5、选择题 沼气是一种能源,它的主要成分是CH4。0.5mol CH4完全燃烧生成CO2和H2O 时,放出445KJ热量,则下列热化学方程式正确的是
时,放出445KJ热量,则下列热化学方程式正确的是
A:2 CH4 (g)+4O2(g)=2CO2(g) +4H2O(l)?△H=+890KJ/mol
B:CH4 +2 O2=CO2+2H2O?△H=-890KJ/mol
C:CH4 (g)+2O2(g)=CO2(g) +2H2O(l)?△H=-890KJ/mol
D:1/2 CH4 (g)+O2( g)= 1/2CO2(g)
g)= 1/2CO2(g)  +H2O(l)?△H=-890KJ/mol
+H2O(l)?△H=-890KJ/mol
参考答案:C
本题解析:略
本题难度:一般