|
高考化学知识点归纳《离子共存》考点预测(2019年强化版)(四)
2019-06-28 21:31:05
【 大 中 小】
|
1、选择题 在pH =1时,可大量共存且形成无色溶液的一组离子或分子是
[? ]
A.Ca2+、CH3COOH、Br-、Na+
B.NO3-、Fe3+、Mg2+、SO42-
C.HClO、Ba2+、Na+、Cl-
D.K+、Cl-、Al3+、SO32-
参考答案:A
本题解析:
本题难度:一般
2、选择题 某课外活动小组的同学从某地颗粒采集器中获得雾霾颗粒样品,然后用蒸馏水浸取。在探究雾霾颗粒可溶性成分的实验中,下列根据实验现象得出的结论不正确的是
A.向浸取液中滴入AgNO3溶液有白色沉淀产生,说明雾霾中一定含有Cl-
B.向浸取液中滴入硝酸酸化的BaCl2溶液,有白色沉淀产生,说明雾霾中一定含SO42-
C.向浸取液中加入Cu和浓H2SO4,试管口有红棕色气体产生,说明雾霾中可能含有NO3-
D.向浸取液中加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明雾霾中一定含有NH4+
|
参考答案:AB
本题解析:A、向浸取液中滴入AgNO3溶液有白色沉淀产生,雾霾中不一定含有Cl-,还可能含有硫酸根、碳酸根等离子,错误;B、向浸取液中滴入硝酸酸化的BaCl2溶液,有白色沉淀产生,雾霾中不一定含SO42-,还可能含有亚硫酸根,错误;C、向浸取液中加入Cu和浓H2SO4,试管口有红棕色气体产生,说明雾霾中可能含有NO3-,正确;D、向浸取液中加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明雾霾中一定含有NH4+,正确。
考点:考查离子检验。
本题难度:一般
3、选择题 一定能在下列溶液中大量共存的离子组是
[? ]
A.含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl-
B.使酚酞变红的溶液:Na+、Ca2+、SO42-、CO32-
C.含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN-
D.含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl-
参考答案:A
本题解析:
本题难度:一般
4、选择题 在无色透明的强碱性溶液中,下列各组离子能大量共存的是(?)
A.
B.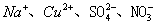
C.
D.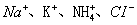
参考答案:A
本题解析:离子间如果发生化学反应,则不能大量共存,反之是可以的。B中铜离子在溶液中显蓝色,不能大量共存;溶液显碱性,C中Mg2+和D中的NH4+不能大量共存,答案选A。
点评:该题是高考中的高频题,属于中等难度的试题,侧重对学生基础知识的训练和检验。有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。该题需要明确离子不能大量共存的一般情况,即(1)能发生复分解反应的离子之间;(2)能生成难溶物的离子之间;(3)能发生氧化还原反应的离子之间;(4)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有:(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。
本题难度:一般
5、填空题 (1)三种弱酸HA、H2B、HC,电离常数为1.8×10-5、5.6×10-11、4.9×10-10、4.3×10-7(数据顺序已打乱),已知三种酸和它们的盐之间能发生以下反应:
①HA+HB-(少量)=A-+H2B?②H2B(少量)+C-=HB-+HC
③HA(少量)+C-=A-+HC
若H2B的Ka1=4.3×10-7,则另二种酸对应的电离常数分别为(根据已知数据填
空):HA的Ka=?,HC的Ka=?。
(2)25 ℃时0.1 mol・L-1的H2R水溶液中,用氢氧化钠来调节溶液pH,得到含有H2R、
HR-、R2-三种微粒的溶液。当c(Na+)=c(R2-)+c(HR-)+c(H2R)时溶液的溶质
为?(填化学式)。
(3)下图是某水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时的组成分数。
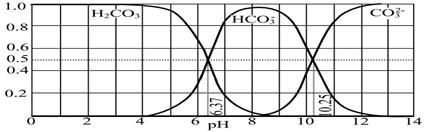
①下列叙述正确的是?。
A.此图是1.0 mol・L-1碳酸钠溶液滴定1.0 mol・L-1 HCl溶液的滴定曲线
B.在pH分别为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-)
C.人体血液的pH约为7.4,则CO2在血液中多以HCO3-形式存在
D.若用CO2和NaOH反应制取NaHCO3,宜控制溶液的pH为7~9之间
②已知Ksp(CaCO3)=5.0×10-9,在10 mL 0.02 mol・L-1的Na2CO3溶液中,加入某浓度的盐酸,调节溶液的pH=10.25,此时溶液的体积恰好为100 mL,向该溶液中加入1 mL 1×10-4 mol・L-1的CaCl2溶液,问是否有沉淀生成??(填“是”或“否”)。
参考答案:(1)HA的Ka=1.8×10-5(1分)、 HC的Ka=4.9×10-10(1分)
(2)NaHR(2分)
(3) ①? C、D(2分)?②?否(2分)
本题解析:(1)由①得出酸性HA强于H2B;由②得H2B强于HC;由③得HA强于HC;HA最强平衡常数最大;(2)该关系式为NaHR的物料守恒;(3)①A、图开始为H2CO3,无碳酸根离子,错误;B、在pH分别为6.37 时c(H2CO3)=c(HCO3-), pH为10.25时,溶液中c(HCO3-)=c(CO32-),错误;C、正确;D、图像中显示pH为7~9之间溶液主要以HCO3-为主,正确;②此时溶液中c(CO32-)=0.02×0.01÷0.1×0.5=0.001mol/L,c(Ca2+)=1×10-4÷100=10-6 mol/L,Q=10-6×0.001=10-9<5.0×10-9,故没有沉淀生成。
本题难度:困难
|