1��ѡ���� Ϊ��ʵ���������������ס��������ڵĹ������к����������ۣ���֪�����ŷŵ���ˮ���������������нϴ�Ũ�ȵ�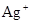 ��
��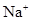 ��
��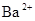 ��
�� ��
��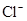 ��
��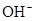 ��
��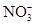 ��
��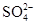 �и�����ͬ���������ӣ��������ŷ��Ի���ɻ�����Ⱦ�������������ˮ���ʵ�������ϣ�����������ˮ�����������Һ�������ж���ȷ���ǣ�?��
�и�����ͬ���������ӣ��������ŷ��Ի���ɻ�����Ⱦ�������������ˮ���ʵ�������ϣ�����������ˮ�����������Һ�������ж���ȷ���ǣ�?��
A��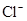 ��
��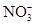 һ�����Բ�ͬ�Ĺ���
һ�����Բ�ͬ�Ĺ���
B��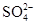 ��
��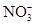 ��������ͬһ����
��������ͬһ����
C��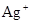 ��
��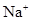 ��������ͬһ����
��������ͬһ����
D��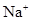 ��
��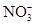 ��������ͬһ����
��������ͬһ����
�ο��𰸣�A
���������Ag����Cl����OH����SO42�������ܴ������棬�������������Ӻ�Ag��һ������ͬһ�����������Ag����NO3����ͬһ������������ΪFe3����OH����Ba2����SO42���ֱ��ܴ������棬���Թ����к��е����ӷֱ���Ag����Ba2����Fe3����NO3����Na����Cl����OH����SO42������ѡA��
�����Ѷȣ�һ��
2��ѡ���� �����и���Һ�У�����һ���ܴ����������
[? ]
A��ǿ������Һ�У�K+��Al3+��Cl-��SO42-
B������0.1 mol��L-1 Fe3+����Һ�У�K+��Mg2+��I-��NO3-
C������0.1 mol��L-1Ca2+��Һ���У�Na+��K+��CO32-��Cl-
D�������£�pH=1����Һ�У�Na+��Fe3+��NO3-��SO42-
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ѡ���� ���б�����ȷ����?��?��
A��̼��������Һ��ˮ�ⷴӦ��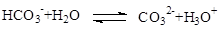
B���ö��Ե缫��ⱥ���Ȼ�þ��Һ��2Cl��+2H2O 2OH��+H2��+Cl2
2OH��+H2��+Cl2
C��������ĵ��뷽��ʽ��H2S=2H++S2-
D����������þ������Һ�еμ��Ȼ�����Һ�����ֺ��ɫ����
�ο��𰸣�D
���������A����CO32-�ĵ��룬B��Mg2+������OH-�������棬����Ӧ������Mg(OH)2��C���Ԫ����ĵ����Ƿֲ��ģ�D����ȷ����ѡD��
������������Ҫ���黯ѧ��������Ƚϼ�����
�����Ѷȣ���
4��ѡ���� ���и�������һ���ܴ���������ǣ�������
A����ɫ��Һ��Ca2+��H+��Cl-��HSO3-
B�������������Ӧ�ų���������Һ�У�K��N03-��Cl-��Fe3+
C��KW/c��H+���T0.1mol/L����Һ��Na+��K+��CO32-��NO3-
D��pH=l����ɫ��Na+��Cu2+��CO32-��NO3-
�ο��𰸣�A����H+��HSO3-�ܽ������ˮ�Ͷ����������壬���ܹ��棬��A��ѡ��
B�������������Ӧ�ų���������ҺΪ���ǿ����Һ������Һ����Fe3+������ɳ��������ܹ��棬��B��ѡ��
C��KW/c��H+���T0.1mol/L����Һ��c��OH-��=0.1mol/L����ҺΪ���ԣ���������֮�䲻��Ӧ���ܹ��棬��Cѡ��
D��pH=1����Һ���д����������ӣ���CO32-�������ˮ�Ͷ�����̼���壬��Cu2+Ϊ��ɫ������ɫ��Һ��������D��ѡ��
��ѡC��
���������
�����Ѷȣ�һ��
5��ѡ���� ����ʵ���ܴﵽԤ��Ŀ�ĵ���
?
| ʵ������
| ʵ��Ŀ��
|
A
| ��1mL0.2mol/LNaOH��Һ�е���2��0.1mol/LMgCl2��Һ��������ɫ�������ٵμ�2��0.1mol/LFeCl3��Һ�������ɺ��ɫ����
| ֤������ͬ�����£��ܽ��Mg(OH)2��Fe(OH)3
|
B
| �����BaCO3������NaOH��Һ�е�����֪Ũ�ȵ����ᣨ�÷�̪��ָʾ����
| �����NaOH����
|
C
| ����һԪ����ҺX��Y��X��pH��Y��l�����ֱ��ˮϡ��l00����pH���
| ֤��ϡ��ǰc(X)��10c(Y)
|
D
| �ⶨ�����ʵ���Ũ�ȵ�HF��HCl��Һ��pH�����߽�С
| ֤���ǽ�����Cl��F
|
?
�ο��𰸣�B
���������A�������������Ȼ�þ��Ӧ�����������ǹ����ģ� ����ٵμ��Ȼ�����Һһ�����ɺ��ɫ�����������������ܵó�������þ�������������ܽ����Դ�С��A����ȷ��B����̪�ı�ɫ��Χ��8.2��10.0����������BaCO3������NaOH��Һ�е�����֪Ũ�ȵ����ᣨ�÷�̪��ָʾ�����ζ���̼�ᱵ����Ӧ�����Բ������������Ƶĺ�����B��ȷ��C������һԪ����ҺX��Y��X��pH��Y��l�����ֱ��ˮϡ��l00����pH��ȣ���˵�����ּ��ͬʱ��ǿ�����Yһ���������˲���ȷ�����ּ��Ũ�ȹ�ϵ��C����ȷ��D���ǽ�����ǿ�����⻯�������ǿ����ϵ����˸��ݵ����ʵ���Ũ�ȵ�HF��HCl��Һ��pH�����߽�С���ܵó��ǽ�����Cl��F��D����ȷ����ѡB��
�����Ѷȣ�һ��