1、填空题 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)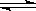 CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
T℃
| 700
| 800
| 830
| 1000
| 1200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
回答下列问题:
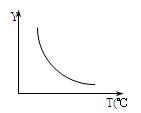
(1)该反应正向为ΔH?0;若该反应符合下图所示的关系,则在图中,Y轴是指?。?
(2)能判断该反应达到化学平衡状态的依据是?(多选扣分)。
a.容器中压强不变?b.混合气体中c(CO)不变
c.v (H2)正=v (H2O)逆?d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式: 0.9・c(CO2)・c(H2)=c(CO)・c(H2O),由此可以判断此时的温度为?℃。其它条件不变,升高温度,原化学平衡向?反应方向移动(填“正”或“逆” ),容器内混合气体的密度?(填“增大”、“减小”或“不变”),气体平均相对分子质量?(填“增大”、“减小”或“不变”)。
),容器内混合气体的密度?(填“增大”、“减小”或“不变”),气体平均相对分子质量?(填“增大”、“减小”或“不变”)。
(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡。若反应开始时CO与H2O的浓度分别为0.200 mol/L和0.100 mol/L,平衡时CO的转化率?。
参考答案:(1)>(1分);CO2或H2的百分含量(1分)(其它合理答案也给分)
(2)b、c (漏选、多选、错选均不得分,2分)
(3)800℃; 正;?不变;?不变(各1分)
(4)33.3%(2分)
本题解析:略
本题难度:简单
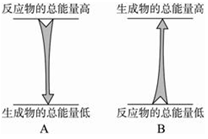
2、选择题 如图是两个反应反应前后反应物总能量和生成物总能量的比较图,对于A、B两个反应的说法正确的是(? )
A.A反应必须加热,B反应不需要加热
B.A反应是放热反应,B反应是吸热反应
C.A反应是吸热反应,B反应是放热反应
D.A反应不需要加热,B反应必须加热
参考答案:B
本题解析:图像分别说明反应物的总能量与生成物的总能量的相对大小,只能说明A为放热反应,B为吸热反应,而反应的条件无从知晓。
本题难度:简单
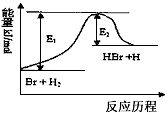
3、选择题 参照反应Br+H2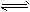 HBr+H的能量对反应历程的示意图,下列叙述中正确的是
HBr+H的能量对反应历程的示意图,下列叙述中正确的是
[? ]
A.该反应的△H=+(E1-E2)kJ/mol
B.加入催化剂,该化学反应的反应热变大
C.反应物总能量高于生成物总能量
D.升高温度可增大正反应速率,降低逆反应速率
参考答案:A
本题解析:
本题难度:一般
4、填空题 如图所示,把试管小心地放入盛有(20 ℃)碳酸饮料的烧杯中,试管中开始放入几小块镁片,再用滴管滴加5 mL稀盐酸于试管中。试回答下列问题:

(1)实验中观察到的现象是?①镁片上有大量气泡产生;②镁片逐渐溶解;③?。(2)产生上述现象的原因是?
(3)由实验推知,MgCl2溶液和氢气的总能量?(填“大于”“小于”或“等于”)镁片和盐酸的总能量。
参考答案:(1)③烧杯中液体放出气泡的速率加快
(2)产生上述现象的原因是:镁与盐酸反应产生氢气,该反应为放热反应,碳酸饮料中CO2气体在水中的溶解度随温度的升高而减小,帮烧杯中液体放出气泡的速率逐渐加快。
(3)小于
本题解析:略
本题难度:简单
5、选择题 下列反应属于吸热反应的是
A.Fe +2HCl = FeCl2十H2↑
B.HCl十NaOH=NaCl十H2O
C.C十H2O 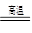 CO十H2
CO十H2
D.CaO十H2O=Ca(OH)2
参考答案:C
本题解析:常见的放热反应:一般的金属与水或酸反应;中和反应;大多数的化合反应和置换反应;一切燃烧反应;缓慢氧化反应。常见的吸热反应:大多数的分解反应,高温下的反应,铵盐与碱反应,C+CO2=2CO,碳、CO和H2做还原剂的反应等。所以A、B、D属于放热反应,C属于吸热反应。所以选C。
点评:反应是吸热还是放热,有些同学还是经常混淆,只从反应类型上看还是不够的,更应该注重从反应物和生成物能量高低上来判断
本题难度:简单