|
高考化学知识点总结《热化学方程式》考点巩固(2019年最新版)(十)
2019-06-28 21:44:13
【 大 中 小】
|
1、填空题 (14分)研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g)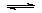 2SO3(g) ΔH= -196.6kJ・mol-1 2SO3(g) ΔH= -196.6kJ・mol-1
2NO(g)+O2(g)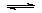 2NO2(g) ΔH= -113.0kJ・mol-1 2NO2(g) ΔH= -113.0kJ・mol-1
则反应NO2(g)+SO2(g)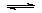 SO3(g)+NO(g)的ΔH= kJ・mol-1。 SO3(g)+NO(g)的ΔH= kJ・mol-1。
一定条件下,将NO2与SO2以体积比2∶1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1molSO3的同时生成1mol NO
| 测得上述反应达平衡时NO2与SO2的体积比为5∶1,则平衡常数K= 。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)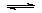 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图(2)所示。该反应ΔH________0(填“>”或“<”)。实际生产条件控制在250℃、 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图(2)所示。该反应ΔH________0(填“>”或“<”)。实际生产条件控制在250℃、
1.3×104kPa左右,选择此压强的理由是: 。
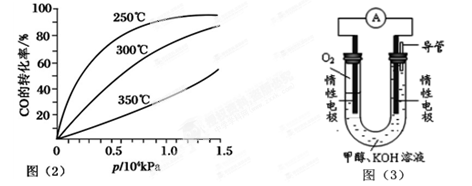
(3)依据燃烧的反应原理,合成的甲醇可以设计如图(3)所示的原电池装置。
① 该电池工作时,OH-向 极移动(填“正”或“负”)。
② 该电池正极的电极反应式为 。
参考答案:(1)-41.8;BD;1.8;
(2)<;在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失;
(3)负极; O2+2H2O+4e-=4OH-;
本题解析:
(1)根据盖斯定律,将第二个方程式反写,与第一个方程式相加得:2NO2(g)+2SO2(g)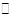 2SO3(g)+2NO(g) 2SO3(g)+2NO(g)
△H="-83.6" kJ?mol-1,则NO2(g)+SO2(g) 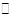 SO3(g)+NO(g) △H="-41.8" kJ?mol-1; SO3(g)+NO(g) △H="-41.8" kJ?mol-1;
A、本反应是反应前后气体分子数不变的反应,故体系的压强保持不变,故A不能说明反应已达到平衡状态;
B、随着反应的进行,NO2的浓度减小,颜色变浅,故B可以说明反应已达平衡;
C、SO3和NO都是生成物,比例保持1:1,故C不能作为平衡状态的判断依据;
D、消耗1molSO3为逆向反应,同时生成1mol NO为正向反应,且满足化学计量数之比,说明正逆反应速率相等,故D能作为平衡状态的判断依据。
NO2(g)+SO2(g) 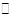 SO3(g)+NO(g) SO3(g)+NO(g)
起始物质的体积 2a a 0 0
转化物质的体积 x x x x
平衡物质的体积 2a-x a-x x x
平衡时NO2(g)与SO2(g)的体积比为5:1,由以上三段式知,(2a-x):(a-x)=5:1,故x=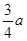 ,故平衡常数K= ,故平衡常数K=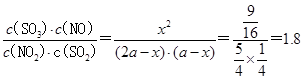 ; ;
(2)由图可知,温度升高,CO的转化率降低,平衡向逆反应方向移动,故逆反应是吸热反应,正反应是放热反应,△H<0;压强大,有利于加快反应速率,有利于使平衡正向移动,但压强过大,需要的动力大,对设备的要求也高,故选择250℃、1.3×104kPa左右的条件.因为在250℃、压强为1.3×104 kPa时,CO的转化率已较大,再增大压强,CO的转化率变化不大,没有必要再增大压强,
(3)①根据原电池的工作原理,阴离子向负极移动,所以OH-向负极移动;
②电解质溶液为碱性溶液,所以正极反应为:O2+2H2O+4e-=4OH-;
考点:考查盖斯定律的应用,热化学方程式的书写,化学平衡标志判断,原电池原理应用
点评:本题考查了盖斯定律的应用,热化学方程式的书写,化学平衡标志判断,原电池原理的应用,难度中等。该题将元素化合物知识与能量变化、化学平衡等知识柔和在一起,综合性较强,需要细细分析,各个突破。易错点是(2),要认真分析图像,得出正确结论。
本题难度:困难
2、填空题 (1)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式: 。
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1 =" ―702" kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2 =" ―182" kJ/mol
由此可知ZnO(s)+Hg(l)= Zn(s)+HgO(s)△H3=  。 。
(3)已知 2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的 ΔH=―99kJ・mol-1.请回答下列问题:
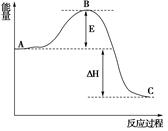
①图中A、C分别表示 、 ,
②E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是
③图中△H= kJ・mol-1。
参考答案:(1)CH4(g)+2O2(g)===CO2(g)+ 2H2O(g) ΔH="-880" kJ/mol
( 2)+260 kJ/mol 2)+260 kJ/mol
(3)①反应物能量 生成物能量
②无 降低 因为催化剂改变了反应的历程使活化能E降低
③-198
本题解析:略
本题难度:简单
3、选择题 下列有关热化学方程式的叙述正确的是( ? )
A.已知CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-893.0kJ/mol,则甲烷的燃烧热为893.0kJ/mol
B.已知4P(红磷,s)=P4(白磷,s);△H>0,则白磷比红磷稳定
C.含20.0g?NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+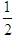 H2SO4(aq)= H2SO4(aq)=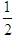 Na2SO4(aq)+H2O(l);△H=-57.4kJ/mol Na2SO4(aq)+H2O(l);△H=-57.4kJ/mol
D.己知C(s)+O2(g)=CO2(g)△H1,C(s)+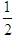 O2(g)=CO(g)△H2,则△H1>△H2 O2(g)=CO(g)△H2,则△H1>△H2
参考答案:C
本题解析:
本题难度:一般
4、填空题 (共7分)工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中的能量变化;请回答下列问题: CH3OH(g)。图1表示反应中的能量变化;请回答下列问题:

(1)在“图1”中,曲线 (填“a”或“b”)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应CO(g)+2H2(g) CH3OH(g)的△H = 。 CH3OH(g)的△H = 。
(2)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)ΔH =-193kJ/mol,又知H2O(l)= H2O(g) ΔH =+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 。
参考答案:(1)b ―91KJ/mol
(2)CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-281kJ/mol
本题解析:(1) 催化剂降低反应的活化能,所以b使用了催化剂;△H =生成物的总能量―反应物的总能量="―91" kJ/mol;(2) ①CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)ΔH =-193kJ/mol,②H2O(l)= H2O(g) ΔH =+44 kJ/mol,根据盖斯定律,①-②×2得:CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-281kJ/mol。
考点:本题考查反应热。
本题难度:一般
5、选择题 下列关于反应能量的说法正确的是
[? ]
A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)? ?ΔH=-216 kJ・mol-1,E反应物<E生成物
B.CaCO3(s)=CaO(s)+CO2(g)? ΔH=+178.5 kJ・mol-1,E反应物<E生成物
C.HI(g)=H2(g)+I2(s) ΔH=-26.5 kJ・mol-1,1 mol HI在密闭容器中分解后放出26.5 kJ的热量
D.H+(aq)+OH-(aq)=H2O(l) ΔH=-57.2 kJ・mol-1,含1 mol NaOH水溶液与含0.5 mol的浓硫酸混合后放热57.2 kJ
参考答案:B
本题解析:
本题难度:简单
|  CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图(2)所示。该反应ΔH________0(填“>”或“<”)。实际生产条件控制在250℃、
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图(2)所示。该反应ΔH________0(填“>”或“<”)。实际生产条件控制在250℃、