1、简答题 已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6.M与其他物质的转化关系如图(部分产物已略去):
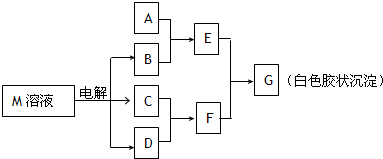
(1)若A是与X、Y同周期的一种常见金属,则A元素在周期表中的位置是______周期______族,写出A与B溶液反应的化学方程式______.
(2)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则该元素原子结构示意图为______,写出E与F反应的离子方程式______.
(3)B的电子式为______,其中的化学键为______.用电子式表示M的形成过程______.
(4)工业上用电解物质M的产物之一氧化有毒含氰(CN-)碱性废水,得到无毒的N2、CO2等.写出此反应的离子反应方程式______.
参考答案:X原子的最外层电子数是最内层电子数的一半,则X是Na元素,X和Y属于同一周期,且Y元素最高正价与它的负价代数和为6,则Y是Cl元素,物质M由同一短周期的X、Y两种元素组成,则M是NaCl,电解氯化钠溶液生成氢气、氯气和氢氧化钠,
(1)若A是与X、Y同周期的一种常见金属,则A是铝,铝能和氢氧化钠反应,则B是氢氧化钠,铝在元素周期表中位于第三周期第IIIA族,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,其反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:第三;IIIA族;2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则A是二氧化硅,所以该元素是硅元素,二氧化硅能和B溶液反应生成E,则B是氢氧化钠溶液,二氧化硅和氢氧化钠溶液生成E硅酸钠,氯气和氢气反应生成F氯化氢,硅酸钠和盐酸反应生成G硅酸,硅原子核外有14个电子,其原子结构示意图为:

,盐酸和硅酸钠反应生成硅酸的离子反应方程式为:2H++SiO32-=H2SiO3↓,
故答案为:

;2H++SiO32-=H2SiO3↓;
(3)B是氢氧化钠,其电子式为:

;?氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,氯化钠的形成过程中钠原子失电子,氯原子得电子,所以氯化钠的形成过程为:

,
故答案为:

;离子键和共价键;

;
(4)氯气氧化氰(CN-)生成N2、CO2,自身被还原生成氯离子,其离子反应方程式为:5Cl2+2CN-+8OH-=10Cl-+N2+2CO2+4H2O,故答案为:5Cl2+2CN-+8OH-=10Cl-+N2+2CO2+4H2O.
本题解析:
本题难度:一般
2、填空题 (7分)某元素的一种同位素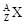 ,其氯化物化学式为XCl2,取该氯化物1.11g
,其氯化物化学式为XCl2,取该氯化物1.11g
溶于水制成溶液后, 加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内质子数与中子数相同,则:
(1)通过计算求得A值(约等于相对原子质量)为?;
(2)X元素在周期表中的位置?;
(3)根据已学知识推测,把X的单质放入水中反应的化学方程式为.?
参考答案:(1) 40(3分) ?(2)第四周期、ⅡA族(2分)? (3) Ca+2H2O="===" Ca(OH)2+H2↑(2分)
本题解析:氯化物和硝酸银反应生成氯化银沉淀,所以根据硝酸银的物质的量可以计算出氯离子的物质的量,即氯离子是0.020L×1mol/L=0.020mol。所以氯化物的物质的量是0.010mol。则其相对分子质量是 ,因此X的质量数是111-35.5×2=40。又因为这种同位素原子核内质子数与中子数相同,所以质子数是20,即是钙元素。钙的金属性其余钠的,和水剧烈反应生成氢氧化钙和氢气。
,因此X的质量数是111-35.5×2=40。又因为这种同位素原子核内质子数与中子数相同,所以质子数是20,即是钙元素。钙的金属性其余钠的,和水剧烈反应生成氢氧化钙和氢气。
本题难度:一般
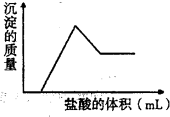
3、选择题 某粉末试样由几种常见氧化物组成.向该粉末试样中加入过量的氢氧化钠溶液,充分溶解后过滤得红棕色固体和无色溶液,向所得无色溶液中滴入盐酸,产生沉淀的质量与所加盐酸的体积的关系如图所示,组成该粉末试样的氧化物可能是( )
A.Fe2O3、MgO、Al2O3
B.Fe2O3、SiO2、Al2O3
C.CuO、SiO2、MgO
D.CuO、MgO、Al2O3