1、选择题 已知短周期元素的离子.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径A>B>D>C
B.a-c=1
C.离子半径C>D>B>A
D.单质的还原性A>B>D>C
参考答案:短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,且A、B在周期表中C、D的下一周期,原子序数:a>b>d>c,A、B为金属,C、D为非金属.
A、A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,原子核外电子层数越多,半径越大,同周期元素原子序数越大,半径越小,则有原子半径:B>A>C>D,故A错误;
B、aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=c+3,即a-c=5,故B错误;
C、aA2+、bB+、cC3-、dD-都具有相同的电子层结构,核电荷数越大,离子半径越小,核电荷数a>b>d>c,所以离子半径C>D>B>A,故C正确;
D、同周期自左而右,金属性减弱,单质还原性减弱,A、B为金属,A、B同周期,a>b,所以金属性B>A;C、D同周期,为非金属,原子序数d>c,非金属性D>C,对应单质的氧化性D>C,所以还原性D<C,故D错误.
故选C.
本题解析:
本题难度:一般
2、选择题 有主族元X、Y、Z,其原子序数依次减小,且均不超过20。X原子的最高能层的电子排布为ns1;Y原子的M能层有2个未成对电子;Z原子的最高能层的p轨道上只有一对成对电子。由这三种元素组成的化合物的化学分子式不可能是
[? ]
A.K2SO3
B.K3PO4
C.K2SiO3
D.K2SO4
参考答案:B
本题解析:
本题难度:一般
3、简答题 A、B、C、D、E、F均为短周期元素,原子序数依次增大,A元素原子核内无中子.B元素原子核外最外层电子数是次外层电子数的2倍.C元素是地壳中含量最多的元素.D是短周期元素中金属性最强的元素.E与D元素的质子数之和为27,最外层电子数之差为5.F元素的最高价氧化物的水化物为强酸.
(1)推断B元素在周期表中的位置:第______周期______族.
(2)写出F元素的电子排布式:______.
(3)C、D元素可形成淡黄色的粉末,其电子式为______,所含化学键为______.
(4)写出A与C元素形成10电子的微粒:______、______、______.
(5)D、E元素形成的正盐的水溶液,阴离子的浓度大小顺序为:(从大到小排列)______.
(6)常温下,1molA元素的单质与C元素的单质化合,放出286kJ的热量.写出反应的热化学方程式:______.
参考答案:A、B、C、D、E、F均为短周期元素,原子序数依次增大.A元素原子核内无中子,则A为氢元素.B元素原子核外最外层电子数是次外层电子数的2倍,则B有2个电子层,最外层有4个电子,则B为碳元素.C元素是地壳中含量最多的元素,则C为氧元素.D是短周期元素中金属性最强的元素,则D为钠元素.E与D元素的质子数之和为27,则E元素的质子数为27-11=16,则E为硫元素.F元素的最高价氧化物的水化物为强酸,原子序数比硫大,则F为氯元素.
即A为氢元素、B为碳元素、C为氧元素、D为钠元素、E为硫元素、F为氯元素.
(1)B为碳元素,原子核外有2个电子层,最外层有4个电子,位于周期表第二周期第ⅣA族.
故答案为:二;ⅣA.
(2)F为氯元素,原子核外有17个电子,电子排布式为1s22s22p63s23p5.
故答案为:1s22s22p63s23p5.
(3)C为氧元素、D为钠元素,二者形成的淡黄色物质为Na2O2,Na2O2是离子化合物,由钠离子与过氧根离子构成,
电子式为
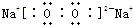
.钠离子与过氧根离子之间形成离子键,过氧根离子中氧原子之间形成1对共用电子对,是非极性共价键.
故答案为:
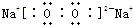
;离子键、非极性共价键.
(4)A为氢元素、C为氧元素,氢元素与氧元素形成10电子的微粒有H2O、H3+O、OH-.
故答案为:H2O、H3+O、OH-.
(5)D为钠元素、E为硫元素,二者形成的正盐为Na2S,属于强碱弱酸盐,所以Na2S的水溶液中,S2-水解S2-+H2O?HS-+OH-,由于水解程度不大,所以离子浓度c(S2-)>c(HS-),由于溶液中存在水的电离,所以c(OH-)>c(HS-),水的电离程度不大,所以c(S2-)>c(HS-),所以阴离子的浓度大小顺序为c(S2-)>c(OH-)>c(HS-).
故答案为:c(S2-)>c(OH-)>c(HS-).
(6)A为氢元素,C为氧元素,常温下,1mol氢气与氧气化合生成液态水,放出286kJ的热量,反应的热化学方程式为H2(g)+12O2(g)=H2O(l);△H=-286kJ/mol.
故答案为:H2(g)+12O2(g)=H2O(l);△H=-286kJ/mol.
本题解析:
本题难度:一般
4、选择题 A、B、C、D四种元素的原子序数依次增大,且均小于18.B、C元素原子的最外层电子数之和等于D元素原子的最外层电子数,A、C同主族且C元素原子的核外电子数是A元素原子核内质子数的两倍.下列叙述不正确的是( )
A.离子半径:C>D>A>B
B.气态氢化物的稳定性:A>C>D
C.B分别与A、C、D可形成四种化合物
D.B分别与A、C、D形成的化合物中只含离子键
参考答案:A、B、C、D四种元素的原子序数依次增大,且均小于18,A、C同主族且C元素原子的核外电子数是A元素原子核内质子数的两倍,则A为O,C为S;B、C元素原子的最外层电子数之和等于D元素原子的最外层电子数,C的最外层电子数为6,则B的最外层电子数为1,D的最外层电子数为7,则B为Na,D为Cl,
A.电子层越多,离子半径越大,具有相同电子排布的离子,原子序数大的离子半径小,则离子半径为C>D>A>B,故A正确;
B.非金属性越强,气态氢化物越稳定,则稳定性为A>D>C,故B错误;
C.B分别与A、C、D可形成四种化合物氧化钠、过氧化钠、硫化钠、氯化钠四种化合物,故C正确;
D.B分别与A、C、D形成的化合物中过氧化钠含有离子键和非极性共价键,故D错误;
故选BD.
本题解析:
本题难度:简单
5、选择题 W粒子的结构示意图如图所示,下列关于它的说法不正确的是( )
A.Y=2
B.若X=18,则Z=8
C.若X=11,它的氧化物化学式为W2O
D.若X=15,它属于金属元素的原子
