1、选择题 下列有关物质分类或归类正确的是
①混合物:盐酸、酒精溶液、水银
②化合物:CaCl2、烧碱、聚苯乙烯、HD
③纯净物:明矾、醋酸溶液、硫酸钡
④同素异形体:C60、C70、金刚石、石墨
A.①③
B.④
C.②③
D.②
参考答案:B
本题解析:①中的水银指Hg,为单质,属于纯净物;②中的HD属于单质;③中醋酸溶液属于混合物;④中C60、C70、石墨、金刚石都是由同种元素组成的单质,互为同素异形体.
本题难度:一般
2、选择题 下列说法正确的是
A.同种元素组成的物质一定是纯净物
B.分子组成相同的物质一定是同种物质
C.混合物是指含有两种或两种以上不同原子的物质
D.组成和结构都相同的分子组成的物质是纯净物
参考答案:D
本题解析:分析:A.由同种元素组成的物质可能是单质、纯净物、混合物;
B.分子式相同结构式不同的化合物为同分异构体;
C.混合物是指由多种物质组成的物质;
D.纯净物是单一的一种物质;
解答:A.由同种元素组成的物质可能是单质、纯净物、混合物,如同素异形体氧气和臭氧混合,是由同种元素组成的混合物,所以由同种元素组成的物质不一定是纯净物,故A错误;
B.分子组成相同的物质不一定是同种物质,如C2H5COOH与CH3COOCH3的分子式相同结构不同,所以它们是同分异构体,但不是同种物质,故B错误;
C.氧气和臭氧的混合物是由同一种元素氧元素混合而成,所以混合物不一定是指含有两种或两种以上不同原子的物质,故C错误;
D.组成和结构决定性质,组成和结构都相同的分子,说明是同种分子,是同一分子,所以组成和结构都相同的分子组成的物质是纯净物,故D正确;
故选D.
点评:本题主要考查了有关物质组成的知识,解答本题分析物质是由几种物质组成,注意对概念的理解和区分,正确从宏观组成和微观构成两个角度来把握,题目难度不大.
本题难度:简单
3、实验题 某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答:
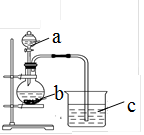
(1)仪器a的名称是?,应盛放下列药品中的?(填序号)。
A.稀硫酸? B. 亚硫酸? C. 氢硫酸? D. 盐酸
(2)仪器b应盛放下列药品中的?(填序号)。
A.碳酸钙? B. 硫酸钠? C. 氯化钠?D. 碳酸钠
(3)b中反应的离子方程式为?。
若看到仪器C中的现象是?,即可证明 ?比??酸性强(填化学式),得电子的能力?比?强。
参考答案:(1)分液漏斗;A(2)D(3)CO32-+2H+=H2O+CO2↑(2分)
澄清石灰水变浑浊?、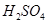 、?
、? 、?硫?、?碳?(各1分)
、?硫?、?碳?(各1分)
本题解析:(1)根据仪器的结构特点可知,a是分液漏斗。要比较它们最高价氧化物对应水化物的酸性强弱,则根据较强的酸制备较弱的原理可知,a中盛放的药品是稀硫酸,答案选A。(2)根据(1)中的分析可知,b中盛放的是碳酸盐。由于硫酸钙是微溶性物质,所以选择的是碳酸钠,答案选D。(3)b是制备CO2的,反应的离子方程式是CO32-+2H+=H2O+CO2↑。CO2能使澄清石灰水变混浊,则C中的实验现象是澄清石灰水变浑浊,据此可知硫酸比碳酸强,S的得到电子的能力强于碳原子的。
本题难度:一般
4、选择题 已知氢有1H、2H、3H三种同位素,氯有35Cl、37Cl两种同位素。用精确的天平分别称量10 000个氯化氢分子,所得数值可能有(?)
A.3种
B.5种
C.6种
D.10 000种
参考答案:B
本题解析:1H、2H、3H分别与35Cl、37Cl结合成1H35Cl、2H35Cl、3H35Cl、1H37Cl、2H37Cl、3H37Cl六种形式,其相对分子质量却只有5种,故称量10 000个HCl分子所得数值为5种。
本题难度:简单
5、选择题 下列事实中,能说明氯的非金属性比硫强的是
A.高氯酸的酸性比亚硫酸强
B.次氯酸的氧化性比稀硫酸强
C.氯化氢比硫化氢的热稳定性好
D.氯原子最外层电子数比硫原子多
参考答案:C
本题解析:A、依据最高价含氧酸的酸性判断非金属性的强弱,高氯酸应与硫酸作比较,错误;B、应比较其简单阴离子的还原性来比较非金属性的强弱,错误;C、利用气态氢化物的稳定性来比较非金属性的强弱,正确;D、依据得电子的难易来比较非金属性的强弱,而不是最外层电子的多少,错误,答案选C。
本题难度:一般