1、选择题 下列说法正确的是( )
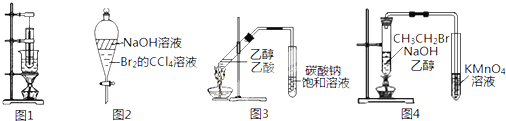
A.图1为实验室制备硝基苯的装置
B.图2中振荡后下层为无色
C.用图3所示的实验装置制备乙酸乙酯
D.图4装置可以达到验证溴乙烷发生消去反应生成烯烃的目的
参考答案:B
本题解析:
本题难度:一般
2、实验题 某化学课外小组用图所示装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
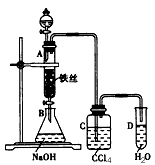
(1)A中反应的化学方程式是__________________。
(2)观察到A中的现象是______________________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是_______________________。有关的化学方程式是____________________________。
(4)C中盛放CCl4的作用是___________________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入__________________,现象是_______________________________________。
参考答案:(1)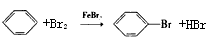
(2)反应液微沸,有红棕色气体充满反应器A
(3)除去溶于溴苯中的溴;Br2+2NaOH=NaBr+NaBrO+H2O
(4)除去HBr气体中的溴蒸气
(5)石蕊试液;溶液变红
本题解析:
本题难度:一般
3、实验题 对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。
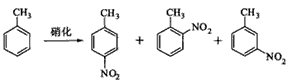
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在溶液中,加入乙酸酐(有脱水作用),45℃反应1h。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(1)上述实验中过滤的目的是____________________。
(2)滤液在分液漏斗中洗涤静置后,有机层处于__________层(填“上”或"下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有____________________。
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。

①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为__________。由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是____________________。
②与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有_______________、______________。
参考答案:(1)回收NaHSO4
(2)下;分液漏斗上口塞子未打开
(3)①0.32;甲苯硝化主要得到对硝基甲苯和邻硝基甲苯;②在硝化产物中对硝基甲苯比例提高;催化剂用量少且能循环使用
本题解析:
本题难度:一般
4、实验题 高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分,实验室可通过下列反应制取
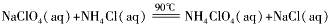
(1)若NH4Cl用氨气和浓盐酸代替,上述反应不需要外界供热就能进行,其原因是________________。
(2)反应得到的混合溶液中NH4ClO4和NaCl的质量分数分别为0.30和0.l5(相关物质的溶解度曲线见下图)。从混合溶液中获得较多NH4ClO4晶体的实验操作依次为(填操作名称)_____________干燥。

(3)样品中NH4ClO4的含量可用蒸馏法进行测定,蒸馏装置如图所示(加热和仪器固定装代已略去),实验步骤如下:
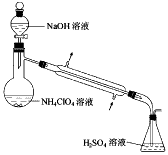
步骤1:按上图所示组装仪器,检查装置气密性。
步骤2:准确称取样品a g(约0.5g)于蒸馏烧瓶中,加入约150mL水溶解。
步骤3:准确量取40.00mL约0.1mol/L H2SO4溶解于锥形瓶中。
步骤4:经滴液漏斗向蒸馏瓶中加入20mL 3mol/LNaOH溶液。
步骤5:加热蒸馏至蒸馏烧瓶中神域约100mL溶液。
步骤6:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用c mol/L NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1mL。
步骤8:将实验步骤1-7重复2次
①步骤3中,准确量取40.00ml H2SO4溶液的玻璃仪器是________。
②步骤1-7中确保生成的氨被稀硫酸完全吸收的实验是_____(填写步骤号)。
③为获得样品中NH4ClO4的含量,还需补充的实验是_____________。
参考答案:(1)氨气与浓盐酸反应放出热量
(2)蒸发浓缩,冷却结晶,过滤,冰水洗涤
(3)①酸式滴定管;②1,5,6;③用NaOH标准溶液标定H2SO4溶液的浓度(或不加高氯酸铵样品,保持其他条件相同,进行蒸馏和滴定实验)
本题解析:
本题难度:困难
5、选择题 下列说法中正确的是?
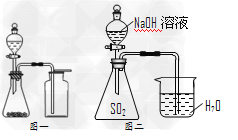
[? ]
A.氯气通入澄清石灰水中,制取漂粉精?
B.可用化合反应的方法制取Fe(OH)3
C.选择合适的试剂,用图一所示装置可分别?制取少量CO2、NO和O2
D.图二装置证明SO2与NaOH发生了反应(系统装置不漏气)
参考答案:B
本题解析:
本题难度:一般