|
高中化学知识点总结《物质制备实验方案的设计》高频考点强化练习(2019年最新版)(二)
2019-06-28 22:00:39
【 大 中 小】
|
1、选择题 下列有关实验操作的叙述正确的是(? )
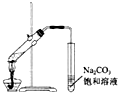
A.实验室常用右上图所示的装置制取少量的乙酸乙酯
B.用50mL酸式滴定管可准确量取25.00mLKMnO4溶液
C.用量筒取5.00mL1.00mol?L-1盐酸于50mL容量瓶中,加水稀释至刻度,可配制0.100mol?L-1盐酸
D.用苯萃取溴水中的溴,分液时有机层从分液漏斗的上口倒出
| 
参考答案:BD
本题解析:
本题难度:简单
2、实验题 实验室可用如图所示装置制取NaClO3。图中:a为氯气发生装 置.b为NaClO3的制备装置;c为尾气吸收装置。请回答下列问题。

(1)制取氯气的化学反应方程式(未配平)为:KMnO4+HCl(浓)→ MnCl2+KCl+Cl2↑+H2O,请将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目。? □+□
(2)开始实验,打开分液漏斗的活塞,发现浓盐酸流出少量后即难以滴下,经检查分液漏斗活塞没有堵塞,你认为应采取的措施是__________。实验时为了除去氯气中的氯化氢气体,可在a与b之间安装盛有_________(填写下列字母编号)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(3)装置b中发生反应的化学方程式为3Cl2 +6NaOH 5NaCl+NaClO3+3H2O,请推测在加热 NaClO溶液时发生反应的化学方程式:____________ 5NaCl+NaClO3+3H2O,请推测在加热 NaClO溶液时发生反应的化学方程式:____________
(4)工业上用石灰乳代替烧碱溶液吸收尾气的原因是__________。工业上用60℃的Na2CO3溶液吸收 Cl2也可制得NaClO3,该反应的离子方程式为_____________ 。
参考答案:(1)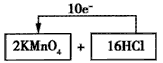
(2)将磨口塞上的凹槽与漏斗口颈上的小孔对准;B
(3)3NaClO2 NaCl+ NaClO3 NaCl+ NaClO3
(4)石灰乳来源丰富、成本低;3Cl2 +3CO32- 5 Cl-+ClO2- +3CO2 5 Cl-+ClO2- +3CO2
本题解析:
本题难度:一般
3、实验题 在如图所示的实验装置中,当A、B、C分别为以下不同组合时,回答有关问题。
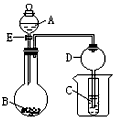
(1)当A为盐酸、B为贝壳(粉末)、C为水玻璃时,小试管中的现象是________________,其中发生的离子反应方程式是________________。
(2)当A为浓氨水、B为生石灰、C为AlCl3溶液,小试管中出现的现象是________________,反应的离子方程式为________________。
(3)当A为浓硫酸、B为Mg、Al、Fe、Cu中的一种银白色片状金属、C为品红溶液,小试管中溶液红色褪去,则B为 (填元素符号), A和B反应的方程式是________________。
(4)装置D的作用是________________。
参考答案:(1)白色胶状物质;SiO32-+CO2+H2O==H2SiO3(胶体)+CO32-
(2)白色沉淀;Al3++3NH3・H2O==Al(OH)3↓+3NH4+
(3)Mg;Mg+2H2SO4(浓)==MgSO4+SO2+2H2O
(4)防倒吸
本题解析:
本题难度:一般
4、选择题 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如下图。下列对该实验的描述错误的是
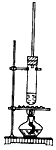
[? ]
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
参考答案:C
本题解析:
本题难度:一般
5、实验题 利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下
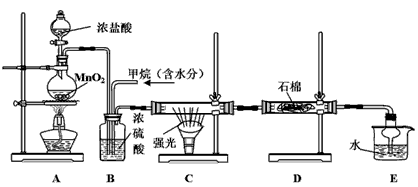
(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③_____________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应≥________。
(3)D装置的石棉中均匀混有KI粉末,其作用是________________。
(4)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式________________。
(5)E装置中除盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为________________。
A.水洗分液法 B.蒸馏法 C.过滤法 D.结晶法
(6)工业上氯气采用电解饱和食盐水的方法来获得。若要获取标况下11.2×103m3的氯气,将同时获得
________ 吨NaOH。
参考答案:(1)干燥气体
(2)4
(3)吸收过量的氯气
(4)
(5)A
(6)40
本题解析:
本题难度:一般
| 