1、填空题 (1)中国古代四大发明之一--黑火药,它的爆炸反应为:2KNO3+3C+S A+ N2↑ +3CO2↑
A+ N2↑ +3CO2↑
①除S外,上列元素的电负性从大到小依次为_______________。
②在生成物中,含极性共价键的分子的中心原于轨道杂化类型为____________。
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为____________
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为_____________,Q2+的未成对电子数是____________
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR-H→Rx[CrCln(H2O)6-n]+xH+ 交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。将含0.001 5 mol[CrCln(H2O)6-n]x+的溶液,与
R-H完全交换后,中和生成的H+需浓度为0.120 0 mol/L NaOH溶液25. 00 mL,可知该配离子的化学式为
___________________
2、填空题 水是自然界中普遍存在的一种物质,根据下列信息回答问题:
(1)氧原子基态时价层电子的电子排布图为_____________。
(2)已知2H2O?=?H3O+?+?OH-,H3O+的立体构型是___________________,中心原子的杂化类型是__________________。
(3)s轨道与s轨道重叠形成的共价键可用符号表示为:δs-s,p轨道与p轨道以“头碰头”方式重叠形成的共价键可用符号δp-p,则H2O分子含有的共价键用符号表示为_________。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低,并说明理由。稳定性_____________理由______________。沸点________________理由:______________。
3、填空题
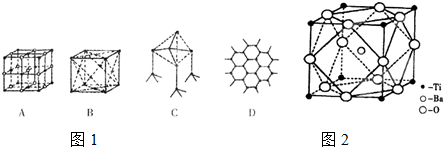
(1)图1所示一些晶体的结构(晶胞),其中代表干冰的是______;
(2)MgO晶胞空间构型与NaCl晶体相同,MgO晶体中Mg2+的配位数为______.与同个Mg2+等距且最近的O2-围成的空间几何构型是______.MgO晶体熔点高于NaCl晶体,原因是______;
(3)若C、D代表某种元素中的两种同分异构体,C中原子的杂化类型是______,属于______晶体.D中原子的杂化类型是______,D能导电的原因是______;
(4)原子晶体能否形成最密堆积结构?______,原因是______;
(5)偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如
图2所示,它的化学式是______.
4、选择题 下列有关甲醛分子的说法中正确的是
[? ]
A.C原子采取sp杂化
B.甲醛分子为三角锥形结构
C.C原子采取sp2杂化
D.甲醛分子为平面三角形结构
5、填空题 以下是表示铁原子和铁离子的3种不同化学用语。
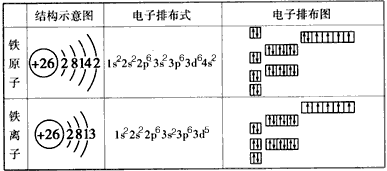
(1)铁原子最外层电子数为_________,铁在参与化学反应时,参加反应的电子可能是___________
(2)请你通过比较、归纳,分别说出3种不同化学用语所能反映的粒子结构信息。
_________________________