1、填空题 (1)中国古代四大发明之一--黑火药,它的爆炸反应为:2KNO3+3C+S A+ N2↑ +3CO2↑
A+ N2↑ +3CO2↑
①除S外,上列元素的电负性从大到小依次为_______________。
②在生成物中,含极性共价键的分子的中心原于轨道杂化类型为____________。
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为____________
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为_____________,Q2+的未成对电子数是____________
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR-H→Rx[CrCln(H2O)6-n]+xH+ 交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。将含0.001 5 mol[CrCln(H2O)6-n]x+的溶液,与
R-H完全交换后,中和生成的H+需浓度为0.120 0 mol/L NaOH溶液25. 00 mL,可知该配离子的化学式为
___________________
参考答案:
(1)①O>N>C>K;②sp;③1:1
(2)3d84s2;4
(3)[CrCl(H2O)5]2+
本题解析:
本题难度:一般
2、填空题 水是自然界中普遍存在的一种物质,根据下列信息回答问题:
(1)氧原子基态时价层电子的电子排布图为_____________。
(2)已知2H2O?=?H3O+?+?OH-,H3O+的立体构型是___________________,中心原子的杂化类型是__________________。
(3)s轨道与s轨道重叠形成的共价键可用 91EXAM.org符号表示为:δs-s,p轨道与p轨道以“头碰头”方式重叠形成的共价键可用符号δp-p,则H2O分子含有的共价键用符号表示为_________。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低,并说明理由。稳定性_____________理由______________。沸点________________理由:______________。
参考答案:(1)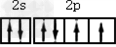 ?
?
(2)三角锥形;sp3?
(3)δs-p?
(4)稳定性:H2O>H2S>H2Se;因为非金属性越强,气态化合物越稳定;沸点:H2O>H2Se>H2S;H2O可形成分子间氢键,沸点最高,H2Se相对分子质量比H2S大,分子间作用力大,因而H2Se比H2S沸点高。
本题解析:
本题难度:一般
3、填空题
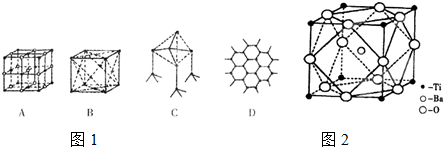
(1)图1所示一些晶体的结构(晶胞),其中代表干冰的是______;
(2)MgO晶胞空间构型与NaCl晶体相同,MgO晶体中Mg2+的配位数为______.与同个Mg2+等距且最近的O2-围成的空间几何构型是______.MgO晶体熔点高于NaCl晶体,原因是______;
(3)若C、D代表某种元素中的两种同分异构体,C中原子的杂化类型是______,属于______晶体.D中原子的杂化类型是______,D能导电的原因是______;
(4)原子晶体能否形成最密堆积结构?______,原因是______;
(5)偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如
图2所示,它的化学式是______.
参考答案:(1)干冰是分子晶体,结合常见晶体可知,其中代表干冰的是B.
故答案为:B.
(2)根据氯化钠的配位数知,氧化镁晶体中镁离子的配位数是6;同个Mg2+等距且最近的O2-围成的空间几何构型是正八面体;电荷越大、离子半径越小其熔点越高,MgO晶体中离子的电荷数大于NaCl,离子间的平均距离小于NaCl,所以MgO晶体熔点高于NaCl晶体.
故答案为:6;正八面体;MgO晶体中离子的电荷数大于NaCl,离子间的平均距离小于NaCl.
(3)C中每个原子含有4个σ键,所以采取sp3杂化,该物质中构成了一个空间网状结构,所以属于原子晶体;
D中每个原子含有3个σ键,所以采取sp2杂化;导体能导电的原因是导体中含有在电流作用下能自由移动的电子,石墨是导体,每个碳原子上未参与杂化的一个2p轨道上电子在层内离域运动(石墨中有自由电子),所以能导电.
故答案为:sp3杂化、原子、sp2杂化、每个碳原子上未参与杂化的一个2p轨道上电子在层内离域运动(石墨中有自由电子).
(4)原子晶体中共价键有饱和性且配位数远小于12,所以不能形成最密堆积结构.
故答案为:不能;共价键有饱和性且配位数远小于12.
(5)该晶胞中含有一个钡原子,含有钛原子个数=8×18=1,含有氧原子个数=14×12=3,所以其化学式为BaTiO3.
故答案为:BaTiO3.
本题解析:
本题难度:简单
4、选择题 下列有关甲醛分子的说法中正确的是
[? ]
A.C原子采取sp杂化
B.甲醛分子为三角锥形结构
C.C原子采取sp2杂化
D.甲醛分子为平面三角形结构
参考答案:CD
本题解析:
本题难度:简单
5、填空题 以下是表示铁原子和铁离子的3种不同化学用语。
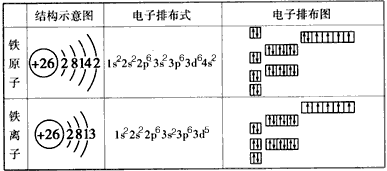
(1)铁原子最外层电子数为_________,铁在参与化学反应时,参加反应的电子可能是___________
(2)请你通过比较、归纳,分别说出3种不同化学用语所能反映的粒子结构信息。
_________________________
参考答案:(1)2;4s上的2个电子(或4s上的2个电子和3d上的1个电子)
(2)结构示意图:能直观地反映原子核内的质子数和核外的电子层数及各能层上的电子数。
电子排布式:能直观地反映粒子核外电子的能层、能级及各能级上的电子数。
电子排布图:能反映粒子各能层、各能级、各轨道的能量的高低及各轨道上的电子分布情况,以及电子的自旋状态。
本题解析:
本题难度:一般