1、选择题 已知aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素正确的是(?)
A.原子半径:A>B>C>D? B.原子序数:b>a>c>d
C.离子半径:D>C>B>A? D.失电子能力:B>A,得电子能力:D>C
2、选择题 中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中错误的是
A.用溶解度数据判断煮沸Mg (HCO3)2溶液得到的产物是Mg(OH)2而不是 MgCO3
B.用沸点数据推测将一些液体混合物用分馏的方法分离开来的可能性
C.利用溶液的pH与7的大小关系,来判断任何温度下溶液的酸碱性
D.用原子(或离子)半径数据推断某些原子(或离子)氧化性或还原性的强弱
3、填空题 (15分)A、B、C、D、E、F六种元素分布在三个不同的短周期,他们的原子序数依次增大,其中 B与C为同一周期,A 与D,C与F分别在同一主族 ,A、D两元素原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体,请回答下列问题:
(1)由A、B两种元素可以组成B2A4型化合物,该化合物中存在的共价键类型为是?。写出该化合物的电子式?
(2)E 是非金属元素,但能表现出一些金属元素的性质,写出E与D元素的最高价氧化物的水化物反应的离子方程式?。
(3)等浓度的ABC2溶液、HClO溶液、盐酸溶液,其导电能力:盐酸溶液>ABC2溶液>HClO溶液,则溶液的 pH (DBC2 )?pH(DClO)(填“>、<、=”)理由是?(用离子方程式解释)
(4)现有100.00mL 未知浓度的ABC2溶液,用?(仪器名称)量取10.00mL待测溶液于锥形瓶中,加入几滴?(可选指示剂:酚酞、石蕊、甲基橙),用A、C、 D三种元素组成的浓度为0.10mol/L的标准溶液来测定未知浓度的ABC2溶液,判断滴定终点的现象是?;记录消耗标准溶液的体积为12.00mL,则该ABC2溶液的浓度为mol/L;
4、选择题 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中W的原子核内质子数与核外最外层电子数之比为8:3,下列说法正确的是
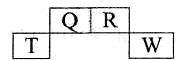
A.T的离子半径大于W的离子半径
B.RHn,在同族元素的气态氢化物中沸点最低
C.Q与W的原子能形成非极性分子
D.在R的最高价氧化物对应水化物的浓溶液中单质T不溶解,说明未发生化学反应
5、选择题 下列每组各有两对物质,它们都能用分液漏斗分离的是
A.四氯化碳和水,酒精和水
B.汽油和水,苯和水
C.甘油和水,乙醇和水
D.醋酸和水,植物油和水